
Verificación del autoanalizador Mindray BS-360E en un hospital universitario de Argentina

Fernandez Machulsky Nahuel (1,2), Fariña Gregorio (1,2), Berg Gabriela (1,2,3).
Filiación: (1) Bioquímica Clínica 1, Departamento de Bioquímica Clínica, Facultad de Farmacia y Bioquímica, Hospital de Clínicas, Universidad de Buenos Aires. (2) Instituto de Fisiopatología y Bioquímica Clínica FFyB-UBA. (3) Consejo Nacional de Investigaciones Científicas y Técnicas.
gaberg@ffyb.uba.ar; Junín 956, CABA, Argentina. Tel: 5411-4964-8297
Resumen
Resumen: La verificación de la precisión intra e inter serie y de la veracidad, son pasos claves e indispensables que debe realizar un laboratorio al incorporar un nuevo equipamiento. En el presente trabajo mostramos la verificación del autoanalizador Mindray BS-360E mediante el protocolo EP-15 A3 y la comparación del mismo con un autoanalizador previamente verificado en nuestro laboratorio, el Cobas c-501 de Roche. Para todos los mensurandos evaluados, la precisión y la veracidad fueron verificadas. Más aún, el rendimiento del autoanalizador Mindray BS-360E fue comparable a la del equipo previamente verificado.
Palabras clave:Verificación de precisión, verificación de veracidad, autoanalizadores, química clínica
Introducción
En el laboratorio de bioquímica clínica, ante la adquisición de un nuevo equipamiento, es esencial la verificación del desempeño analítico de los mensurandos antes de proceder a analizar las muestras de los pacientes (1). Este constituye la verificación de la precisión, veracidad, límite de deteccion y cuantificacion, valores de referencia, linealidad e incertidumbre (2)
El Clinical and Laboratory Standards Institute (CLSI) propone los procedimientos a realizar por los laboratorios a fin de realizar esta verificación. Entre ellas se encuentran la Evaluation Procedure 15 versión 3 (EP15A3) (3) y la Evaluation Procedure 9 versión 2 (EP9A2) (4).
EP15A3, es un procedimiento que permite tanto la verificación de la precisión intra e inter-serie como la verificación de la veracidad, y puede ser aplicado en laboratorios de distinta complejidad, independientemente de sus recursos. Brevemente, se deben procesar al menos dos niveles de una muestra con concentraciones conocidas de los mensurandos a verificar. Estas muestras deben ser medidas por quintuplicado durante 5 días consecutivos (Figura 1). A partir de los resultados obtenidos se calculan los coeficientes de variación (CV%) intra e inter ensayo, los cuales se comparan con los declarados por el fabricante con el objetivo de verificar la precisión. En referencia a la veracidad, lo recomendado es la utilización de un material con valores asignados, cercanos a los niveles de decisión médica y a los especificados por el fabricante en los que éste determinó las especificaciones de precisión declarada. A partir de los resultados obtenidos, se los compara con los resultados del material con valor asignado a fin de obtener el sesgo, el cual tiene que ser menor al propuesto por el laboratorio donde se adquirió el equipamiento a evaluar.

Con respecto a la EP9A2, esta tiene como objetivo la comparación del equipo adquirido versus un equipamiento de referencia previamente verificado. En este caso se deben procesar en ambos equipos simultáneamente, al menos 40 muestras por duplicado que abarquen el mayor rango de concentración posible para los mensurandos a evaluar. Teniendo en cuenta los requisitos de calidad del laboratorio en cuestión se realiza la regresión de Passing Bablok (5) y el análisis de Bland Altman (6). Previo a la verificación de todo nuevo equipamiento, es necesario calibrar el sistema de medición de acuerdo a las especificaciones del fabricante, así como aprobar los controles de calidad interno provistos por el mismo según protocolos establecidos por el propio laboratorio.
En el año 2023, nuestro laboratorio incorporó un autoanalizador de química clínica Mindray BS-360E, equipo de mesada de muy fácil manejo, con 360 test/hora. El equipo tiene la ventaja que permite calibración lineal, con dos y múltiples puntos; tiene incorporadas las reglas de Westgard, el gráfico de Levey-Jennings y la comprobación de suma acumulada así como el gráfico de Youden.
Objetivo
Realizar la verificación del autoanalizador BS-360E mediante el protocolo EP15A3 y la comparación con el autoanalizador Roche Cobas c-501 previamente verificado el cual se utiliza en la práctica diaria en nuestro laboratorio.
Materiales y Métodos
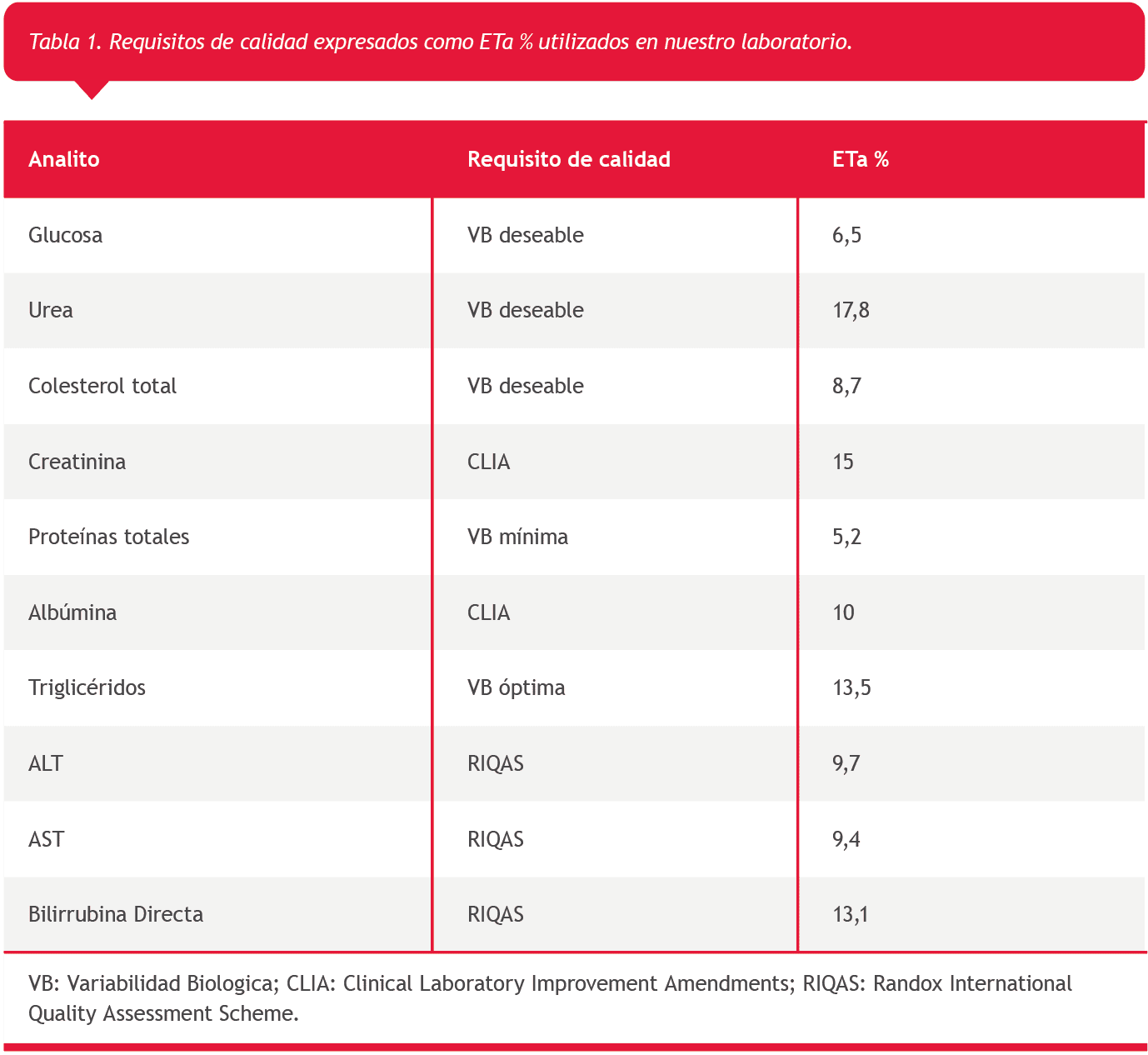
Se realizó el protocolo EP15A3 para los siguientes mensurandos utilizando dos niveles de un control de calidad de tercera opinión (Lyphochek® Assayed Chemistry Control-Biorad): albúmina (Verde de bromocresol), aspartato aminotransferasa (AST) (UV según IFCC sin activación por fosfato de piridoxal), alanina aminotransferasa (ALT) (UV según IFCC sin activación por fosfato de piridoxal), bilirrubina directa (ácido sulfanílico diazotado), colesterol total (colesterol oxidasa-peroxidasa), creatinina (sarcosina oxidasa), glucosa (glucosa oxidasa-peroxidasa), proteínas totales (Biuret), triglicéridos (glicerol quinasa- oxidasa -peroxidasa) y urea (ureasa-glutamato deshidrogenasa UV), comparando los resultados de precisión con las afirmaciones del fabricante y de veracidad con los errores totales aceptables (ETa %) utilizados en nuestro laboratorio (Tabla 1).
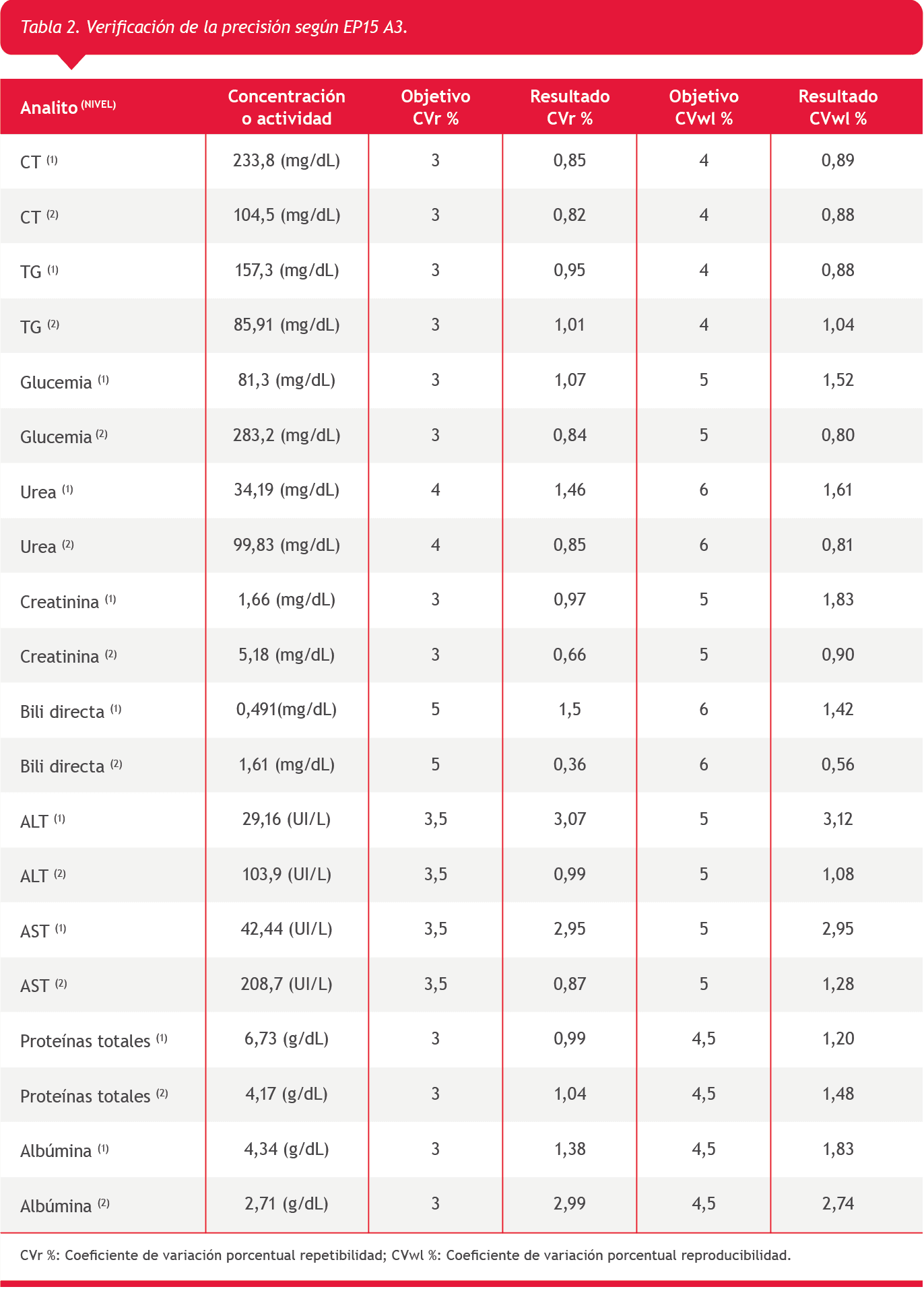
Se calcularon y cotejaron las estimaciones de imprecisión (CV%) intra-ensayo (repetibilidad) y entre-ensayos (reproducibilidad). En cuanto a la verificación de la veracidad se comparó la media de las mediciones obtenida con el valor objetivo y el intervalo de verificación, se calculó la incertidumbre máxima expandida, el sesgo y se los comparó con el sesgo máximo permitido según ETa % de la Tabla 1.
Por su parte, a fin de realizar la comparación entre autoanalizadores se siguió las recomendaciones de EP9A2 con la salvedad de que las muestras se procesaron una única vez y no por duplicado. De este modo, se procesaron al menos 40 muestras en ambos equipos para los analitos descritos, con excepción de albúmina. Con los resultados obtenidos se llevó a cabo el análisis de regresión de Passing Bablok y el análisis de Bland Altman.
Resultados
Como podemos observar en la Tabla 2, los hallazgos de nuestro estudio de repetibilidad y reproducibilidad en el autoanalizador Mindray BS-360E mostraron que la totalidad de los mensurandos evaluados, en ambos niveles de concentración, verificaron los requisitos propuestos por el fabricante, encontrándose en todos los casos claramente por debajo del límite sugerido.
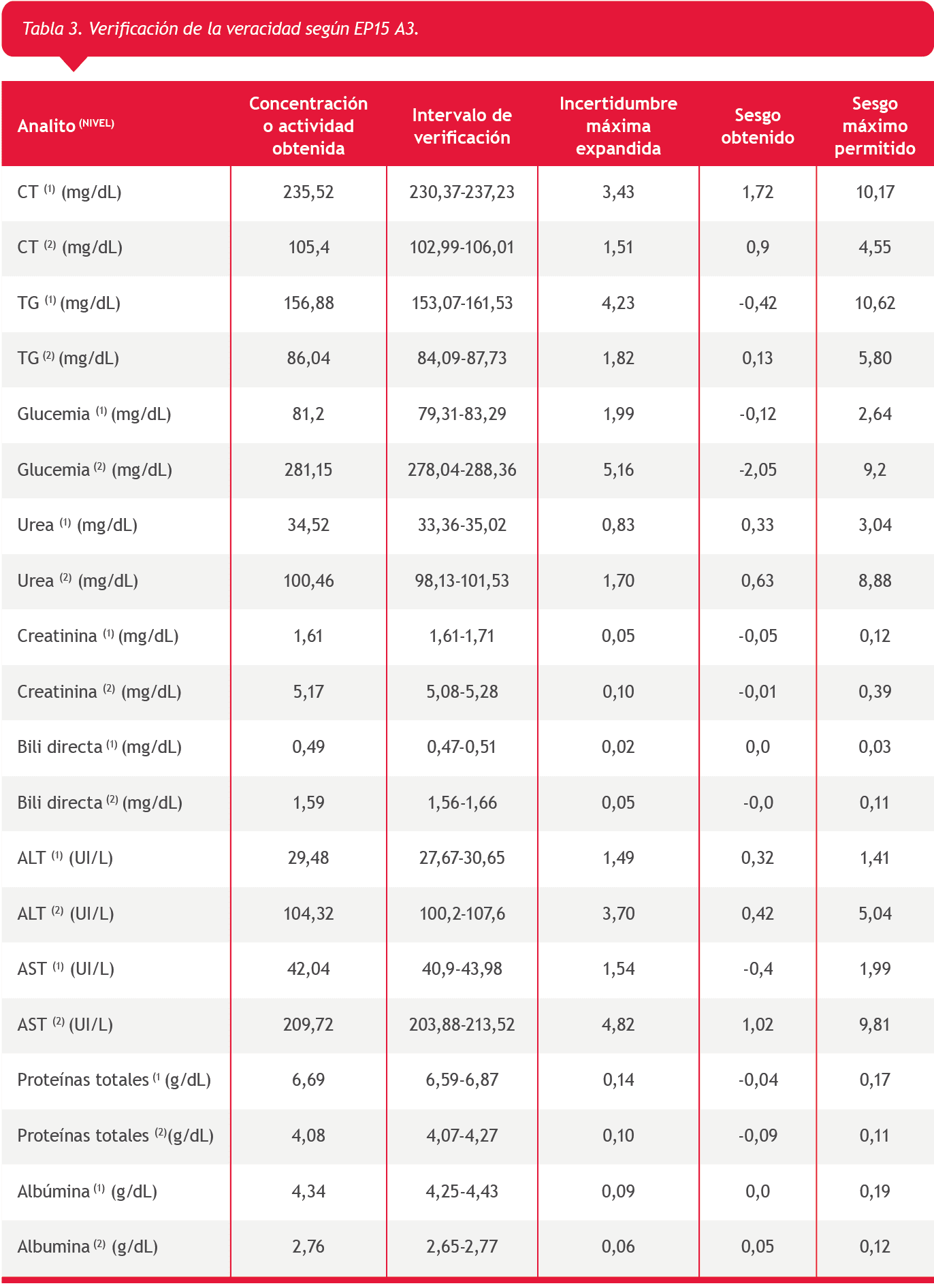
Con respecto a la veracidad, en la Tabla 3 se observa la media de los resultados obtenidos para cada mensurando y su rango de aceptabilidad, el cual fue aprobado en todos los casos. A continuación se describe la incertidumbre máxima expandida, el sesgo obtenido y el sesgo objetivo. Solamente la actividad 1 de ALT mostró una incertidumbre máxima expandida ligeramente mayor a la esperada según nuestros requisitos de calidad.
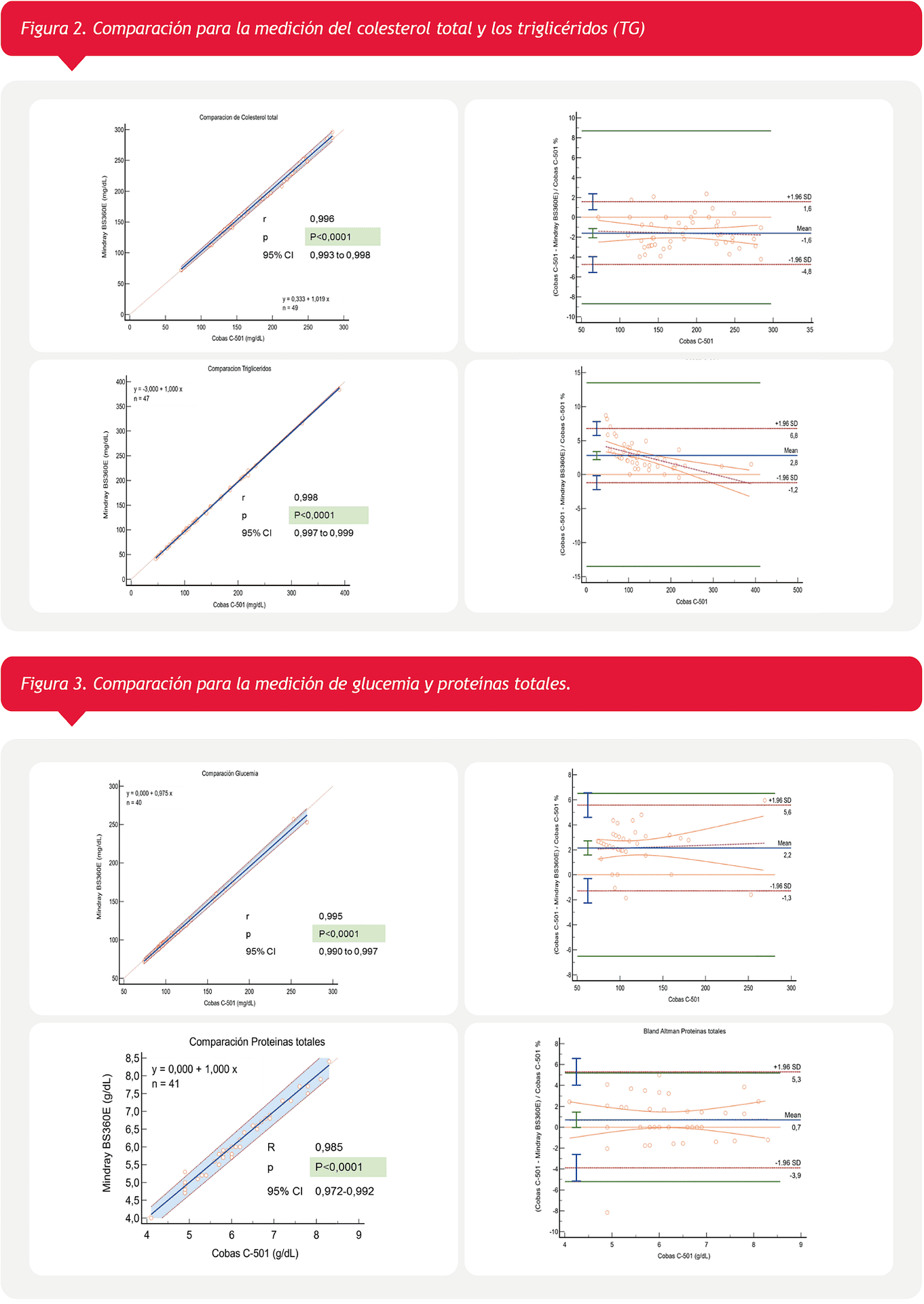
En la figura 2 se observan los resultados obtenidos en la comparación entre el Mindray BS-360E y el Cobas c-501 para la medición del colesterol total y los triglicéridos (TG). En ambos casos se observa una excelente correlación, con sesgos menores a los estipulados por nuestro laboratorio. En el caso de los TG se observa que la diferencia entre ambos autoanalizadores es dependiente de la concentración, con una tendencia a la sobreestimación de TG por el BS-360E a medida que aumenta la concentración del mismo.
En cuanto a la glucemia y las proteínas totales (Figura 3), observamos que ambos presentan una muy buena correlación y sesgo acorde al esperado según ETa %, a sabiendas que los métodos de glucemia comparados fueron diferentes (Hexoquinasa vs oxidasa-peroxidasa).
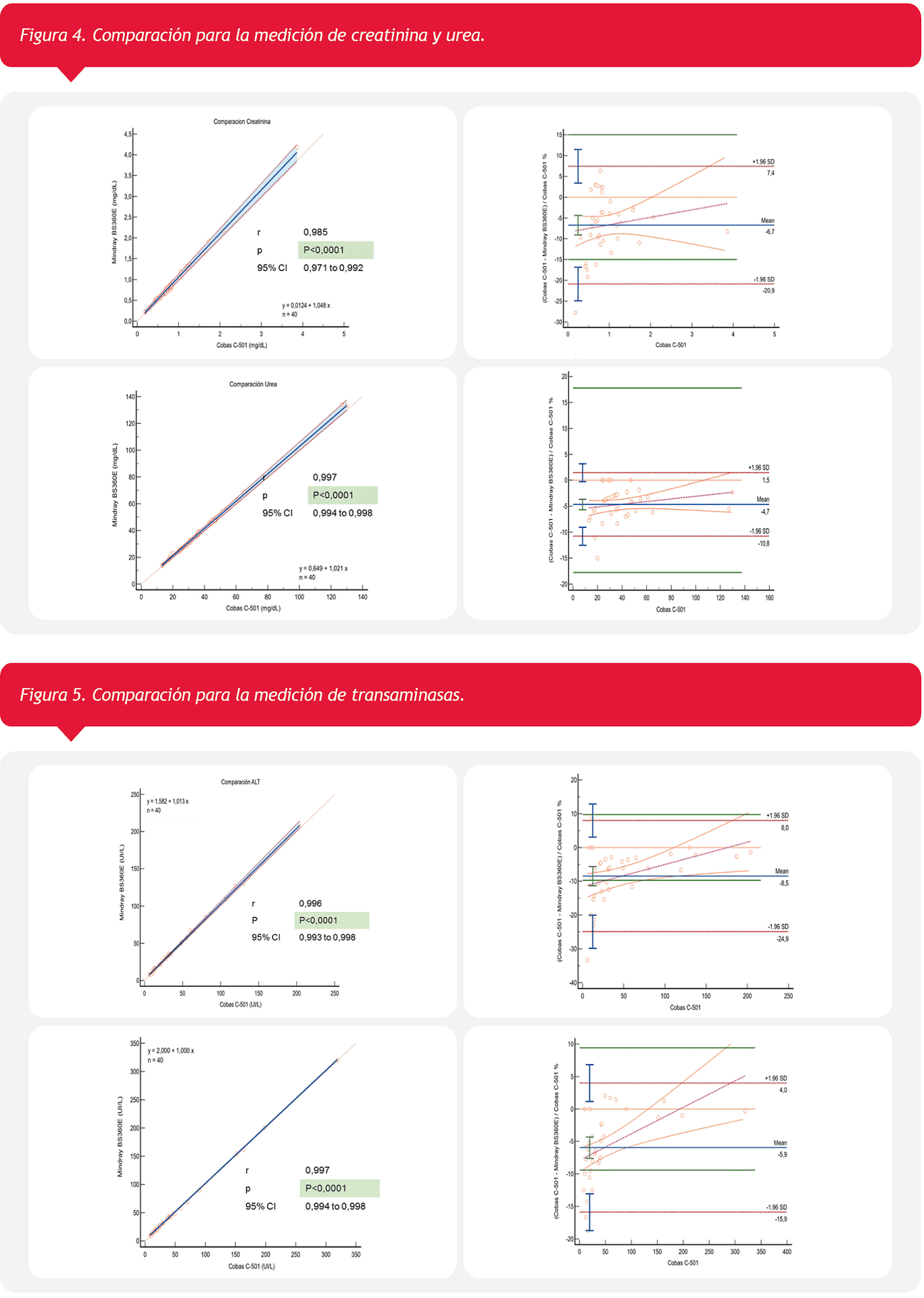
La creatinina medida en c-501 fue por la metodología Jaffe cinético, sin embargo la diferencia con el BS-360E fue menor al sesgo propuesto, si bien se observa que a medida que aumenta la concentración, la medición con este último tiende a subestimar en comparación con el c-501. Esto mismo vemos que sucede con la urea, aunque en este caso, en ambas plataformas fue medido con la misma técnica (Figura 4).
En cuanto a las transaminasas (Figura 5), en ambos casos se observa una tendencia a la subestimación a medida que aumenta la actividad, sin embargo, en los respectivos intervalos de referencia se observa lo opuesto, una sobreestimación por parte de BS-360E con respecto al c-501.
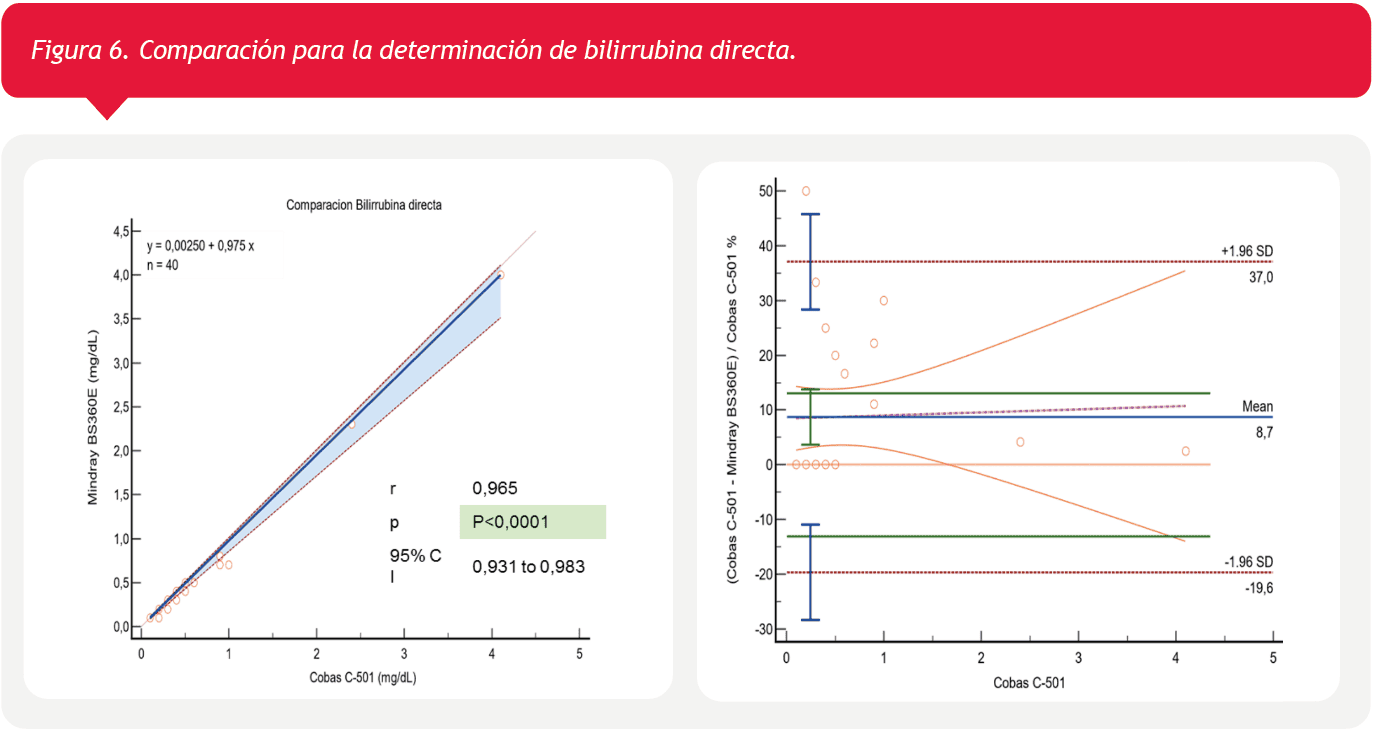
Finalmente la comparación de la bilirrubina directa, la cual se observa una tendencia a la subestimación por BS-360E en valores normales (Figura 6).
Discusión
En el laboratorio de bioquímica clínica, la evaluación de la precisión y veracidad de un autoanalizador es un paso fundamental para la correcta utilización del mismo en la práctica diaria. Luego de llevar a cabo el protocolo EP15A3 en nuestro laboratorio, hemos comprobado que el autoanalizador Mindray BS-360E, cumple con el desempeño de precisión indicado por el fabricante con un sesgo menor al presupuesto de error del laboratorio para los mensurando analizados. La comparación con el equipo Cobas c-501 mostró resultados satisfactorios para todos los analitos evaluados. La bilirrubina directa mostró una subestimación con BS-360E en pacientes con bilirrubina directa normal, sin embargo, ninguno de estas diferencias tuvo implicancias clínicas, dado que todos los pacientes clasificados con bilirrubina normal con c-501 fueron clasificados con bilirrubina normal con BS-360E.
Conclusión: Debido a lo estudiado y a lo establecido por nuestro laboratorio, se ha verificado la precisión y la veracidad del autoanalizador Mindray BS-360E y se ha comparado su rendimiento contrastando al equipamiento verificado utilizado a diario.
Referencias Bibliográficas
1. Fundación Bioquímica Argentina. Manual de acreditación Nº 3. 2012. Comité Ejecutivo del Programa de Acreditación de Laboratorios.
2. Clinical and Laboratory Standards Institute. EP-19: Evaluation of precision of quantitative measurement methods; approved guideline. 2020. Clinical and Laboratory Standards Institute.
3. Clinical and Laboratory Standards Institute. EP15 A3: User protocol for evaluation of qualitative test performance; approved guideline—third edition. 2014. Clinical and Laboratory Standards Institute.
4. Clinical and Laboratory Standards Institute (CLSI). EP9 A2: Measurement Procedure Comparison and Bias Estimation; approved guideline—second guideline. 2018. Clinical and Laboratory Standards Institute.
5. Passing H, Bablok W. A new biometrical procedure for testing the equality of measurements from two different analytical methods. J Clin Chem Clin Biochem. 1983;21(11):709–720.
6. Bland JM, Altman DG. Statistical methods for assessing agreement between two methods of clinical measurement. Lancet. 1986;1(8476):307–310.





