
Síntesis de la evidencia: Guía de práctica clínica para el diagnóstico y el tratamiento de la pubertad precoz
Boletín Médico del Hospital Infantil de México
M. Fernanda Castilla-Peón1*, Margarita Torres-Tamayo2, Jessie N. Zurita-Cruz3, Blanca E. Aguilar-Herrera4, América L. Miranda-Lora1, Aleida J. Rivera-Hernández4, Raúl Calzada-León5, Marco A. Morales-Pérez6, Miriam M. Padrón-Martínez5, María L. Ruiz-Reyes5, Leticia M. García-orales1, Consuelo Barrón-Uribe3, Sletza L. Arguinzoniz-Valenzuela5, Mayra C. Torres-Castañeda7, Lorena Lizárraga-Paulin7, Jorge A. Núñez-Hernández8,9, Judith Cornejo-Barrera10, María T. Vidal-González11, María R. Martínez-Alvarado2, Elisa Nishimura-Meguro3, Luz E. Bravo-Ríos3, Eulalia P. Garrido-Magaña4, José A. Orozco-Morales1, Patricia G. Medina-Bravo1 y Ninel Coyote-Estrada3
1Hospital Infantil de México Federico Gómez, Ciudad de México; 2Instituto Nacional de Cardiología Ignacio Chávez, Ciudad de México; 3Hospital de Pediatría Centro Médico Nacional Siglo XXI, Ciudad de México; 4Sociedad Mexicana de Endocrinología Pediátrica, Ciudad de México; 5Instituto Nacional de Pediatría, Ciudad de México; 6Hospital General de Zona No. 18, Playa del Carmen, Quintana Roo; 7Hospital General del Centro Médico Nacional La Raza, Ciudad de México; 8Hospital General Regional 220, Instituto Mexicano del Seguro Social, Ciudad de México; 9Instituto Materno Infantil del Estado de México, Toluca, Estado de México; 10Hospital Infantil de Tamaulipas, Ciudad Victoria, Tamaulipas; 11Hospital del Niño y el Adolescente Morelense, Cuernavaca, Morelos. México
Correspondencia: *M. Fernanda Castilla Peón – E-mail: fernandacastillapeon@gmail.com – Disponible en internet: 23-06-2020 – Bol Med Hosp Infant Mex. 2020;77(Supl 1):35-40 – www.bmhim.com – DOI: 10.24875/BMHIM.20000087 – 1665-1146/© 2020 Hospital Infantil de México Federico Gómez. Publicado por Permanyer. Este es un artículo open access bajo la licencia CC BY-NC-ND – (http://creativecommons.org/licenses/by-nc-nd/4.0/).
Resumen
Se realizaron tres revisiones sistemáticas para la formulación de las recomendaciones sobre diagnóstico, tratamiento y seguimiento de pacientes con pubertad precoz: intervenciones para el tratamiento de la pubertad precoz que incluyeran los desenlaces de talla final o casi final, salud mental, salud metabólica, salud ósea o éxito en el bloqueo; estudios observacionales comparativos que evaluaran desenlaces a largo plazo en sujetos con antecedentes de pubertad precoz; y por último, estudios de exactitud de prueba diagnóstica para pubertad.
Palabras clave: Pubertad precoz, Tratamiento, Diagnóstico, Revisión sistemática.
Synthesis of the evidence: Clinical guideline for the diagnosis and treatment of precocious puberty
Abstract
Three systematic reviews were conducted to formulate the recommendations on diagnosis, treatment and follow-up of patients with precocious puberty: interventions for the treatment of precocious puberty that included the outcomes of final or near-final height, mental health, metabolic health, health bone, or blockade success; comparative observational studies evaluating long-term outcomes in subjects with a history of precocious puberty; and diagnostic test accuracy studies for puberty.
Key words: Precocious puberty, Treatment, Diagnosis, Systematic review.
Análogos de la hormona liberadora de gonadotropina (aGnRH) para el tratamiento de la pubertad precoz
Metodología
Criterios de inclusión
– Tipo de estudios: ensayos clínicos controlados con o sin aleatorización y con o sin cegamiento que evaluaran cualquiera de los desenlaces de interés. Se buscaron también estudios observacionales comparativos que evaluaran alguno de los desenlaces de interés en la edad adulta.
– Tipo de participantes: niñas menores de 8 años con crecimiento mamario (estadio de Tanner II o mayor) y niños menores de 9 años con crecimiento testicular (volumen testicular de 4 cm3 o mayor).
– Intervención: algún aGnRH de depósito (triptorelina, leuprorelina, histrelina o goserelina) con o sin cointervenciones.
– Control: sujetos que no recibieron aGnRH o que recibieron una dosis o una formulación diferente de las del grupo de intervención. En caso de que se usaran cointervenciones, ambos grupos debían haber recibido las mismas.
– Desenlaces: talla adulta o casi adulta, medidas de impacto psicológico o de calidad de vida, medidas de éxito en el bloqueo de la pubertad, medidas de salud ósea y medidas de salud metabólica.
Estrategia de búsqueda
– Ensayos clínicos: se realizó una búsqueda en Pub-Med y Cochrane Library Trials Register con los términos “puberty” AND (“GnRH analog” OR “GnRH agonist” OR “gonadotropin releasing hormone agonist” OR “gonadotropin releasing hormone analog” OR “gonadotropin-releasing hormone agonist” OR “gonadotropin-releasing hormone analog” OR “leuprolide” OR “triptorelin” OR “histrelin” OR “goserelin” OR “nafarelin”). Filtro: ensayos clínicos.
– Estudios observacionales a largo plazo: se realizó una búsqueda en PubMed con los términos “puberty AND (“GnRH analog” OR “GnRH agonist” OR “gonadotropin releasing hormone agonist” OR “gonadotropin releasing hormone analog” OR “gonadotropin-releasing hormone agonist” OR “gonadotropin-releasing hormone analog” OR “leuprolide” OR “triptorelin” OR “histrelin” OR “goserelin” OR “nafarelin”) AND (“adult height” OR “final height” OR “adverse events” OR “side effects” OR “safety” OR “bone” OR “metabolic” OR “lipids” OR “insulin resistance”).
Filtros: clinical trial phase III, clinical trialphase IV, comparative study, observational study.
También se realizó la búsqueda con los términos (“precocious puberty” [title] AND (“GnRH” OR “treatment”) AND (“long term” OR “adult”).
– Desenlaces psicosociales: por ser de particular interés, también se llevó a cabo una búsqueda para los desenlaces psicosociales en PubMed con los términos “Puberty, precocious” AND (“mental health” OR “quality of life” OR “psychological” OR “health risk behaviors”). Filtro: español e inglés.
Selección de estudios
Todos los títulos y los resúmenes identificados en la búsqueda fueron evaluados por dos revisores, quienes examinaron el texto completo de todos los ensayos que potencialmente cumplían los criterios de inclusión. Se resolvieron los desacuerdos mediante discusión con un tercer revisor hasta llegar a un consenso.
Extracción de datos
Dos revisores por estudio extrajeron los datos relevantes de los estudios en un formato diseñado previamente. Cuando hubo discordancia en la captura de datos, se discutió con un tercer revisor hasta llegar a un consenso.
Evaluación de la calidad de los estudios incluidos
Se evaluó el riesgo de sesgo mediante la herramienta Programa de Habilidades de Lectura Crítica en Español (CASPe, Critical Appraisal Skills Programme – español) para ensayos clínicos1. Una vez considerados los rubros evaluados por este instrumento, los miembros del grupo desarrollador de la guía asignaron uno de tres niveles para la calidad (de menor a mayor): −, + y ++.
Resultados
Ensayos clínicos
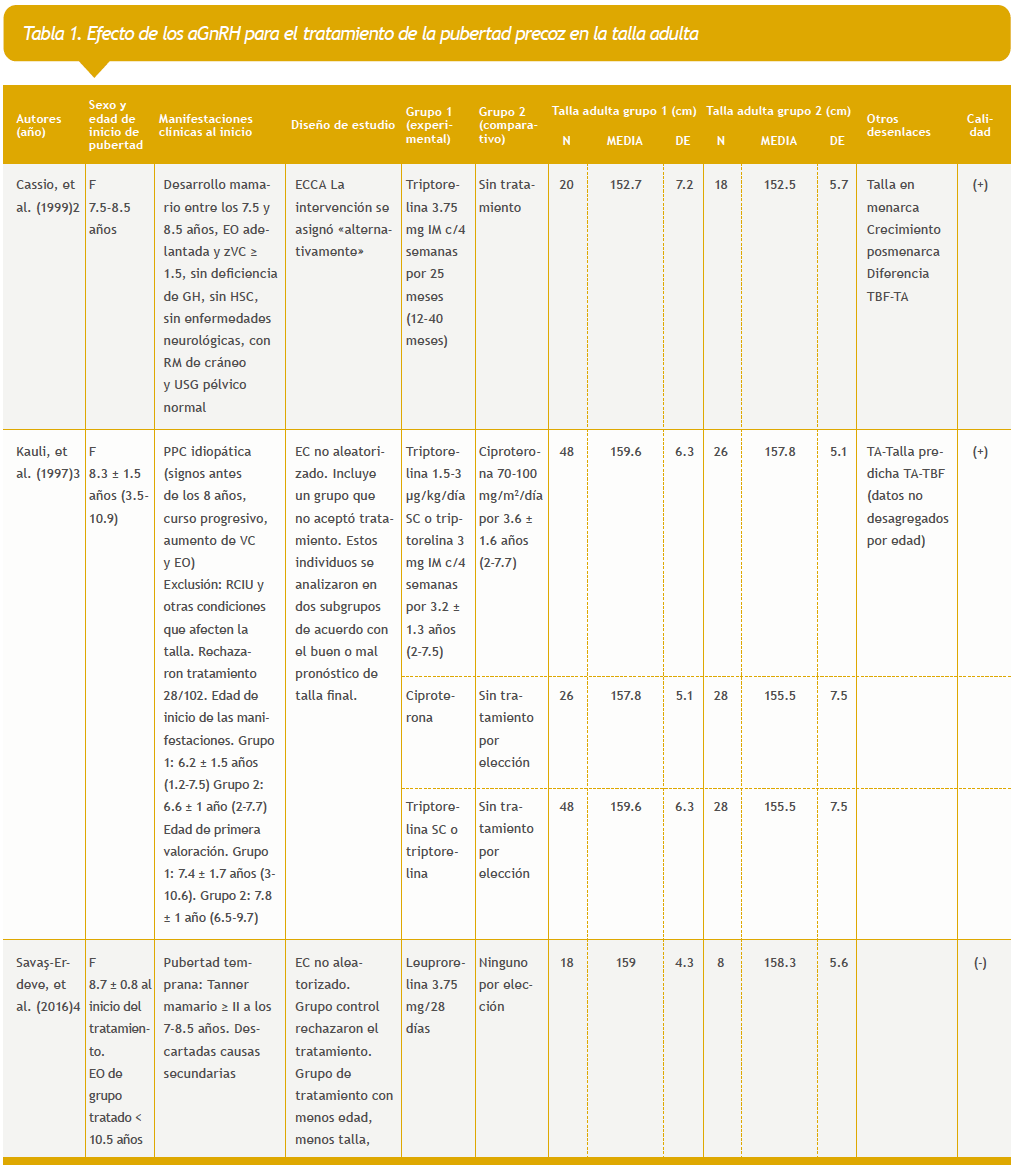
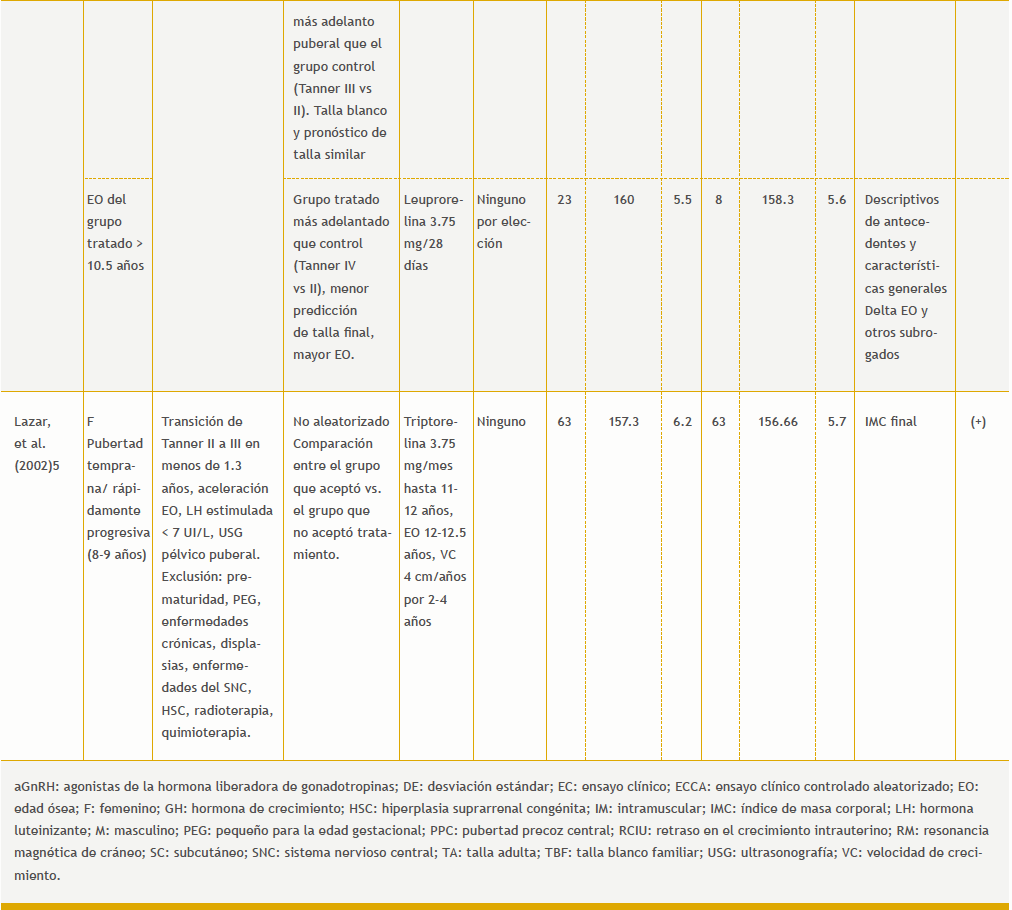
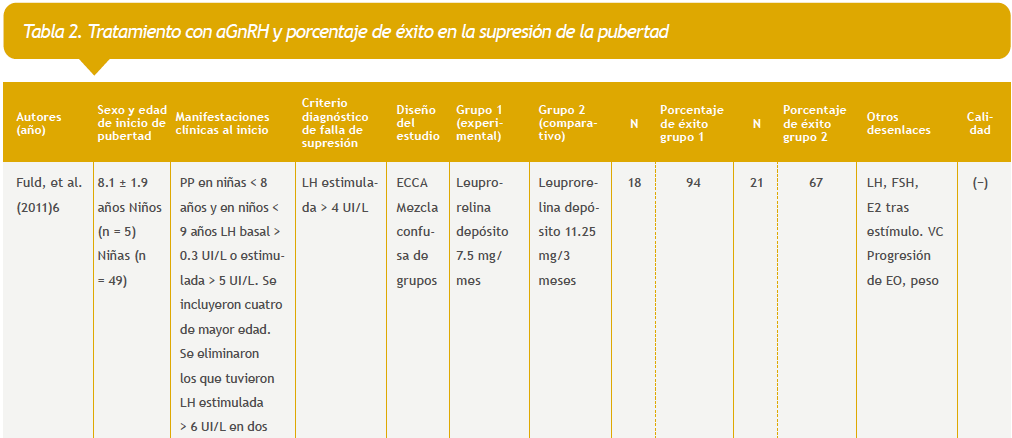
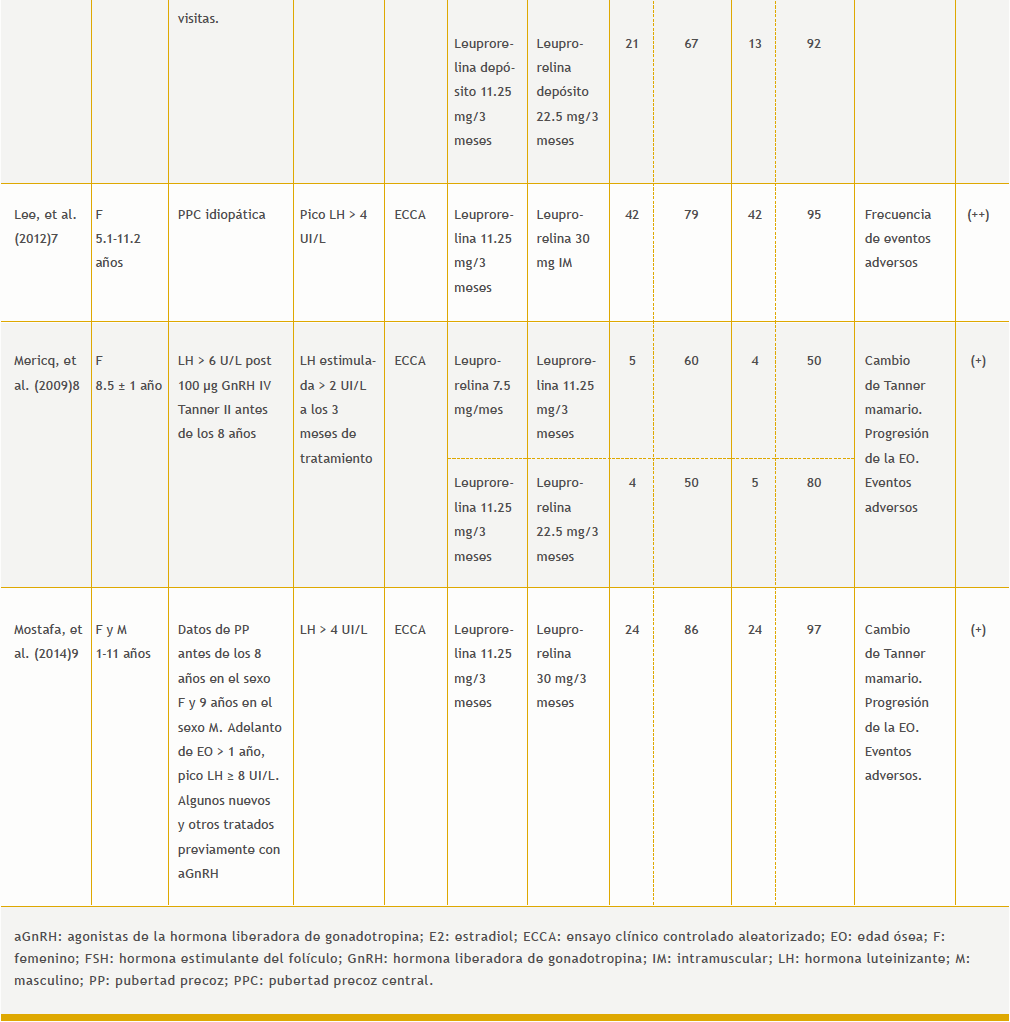
Se identificaron 78 referencias en el Registro de Ensayos Clínicos de Cochrane Library y 88 referencias en PubMed hasta el 6 de marzo de 2018. Se excluyeron 30 referencias por estar duplicadas. Ocho estudios cumplieron los criterios de inclusión. Los estudios incluidos se describen en las tablas 1 y 2 del anexo.
Estudios observacionales a largo plazo
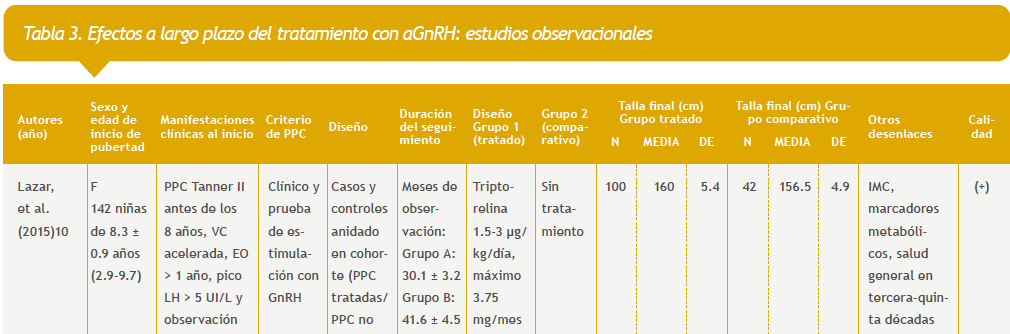
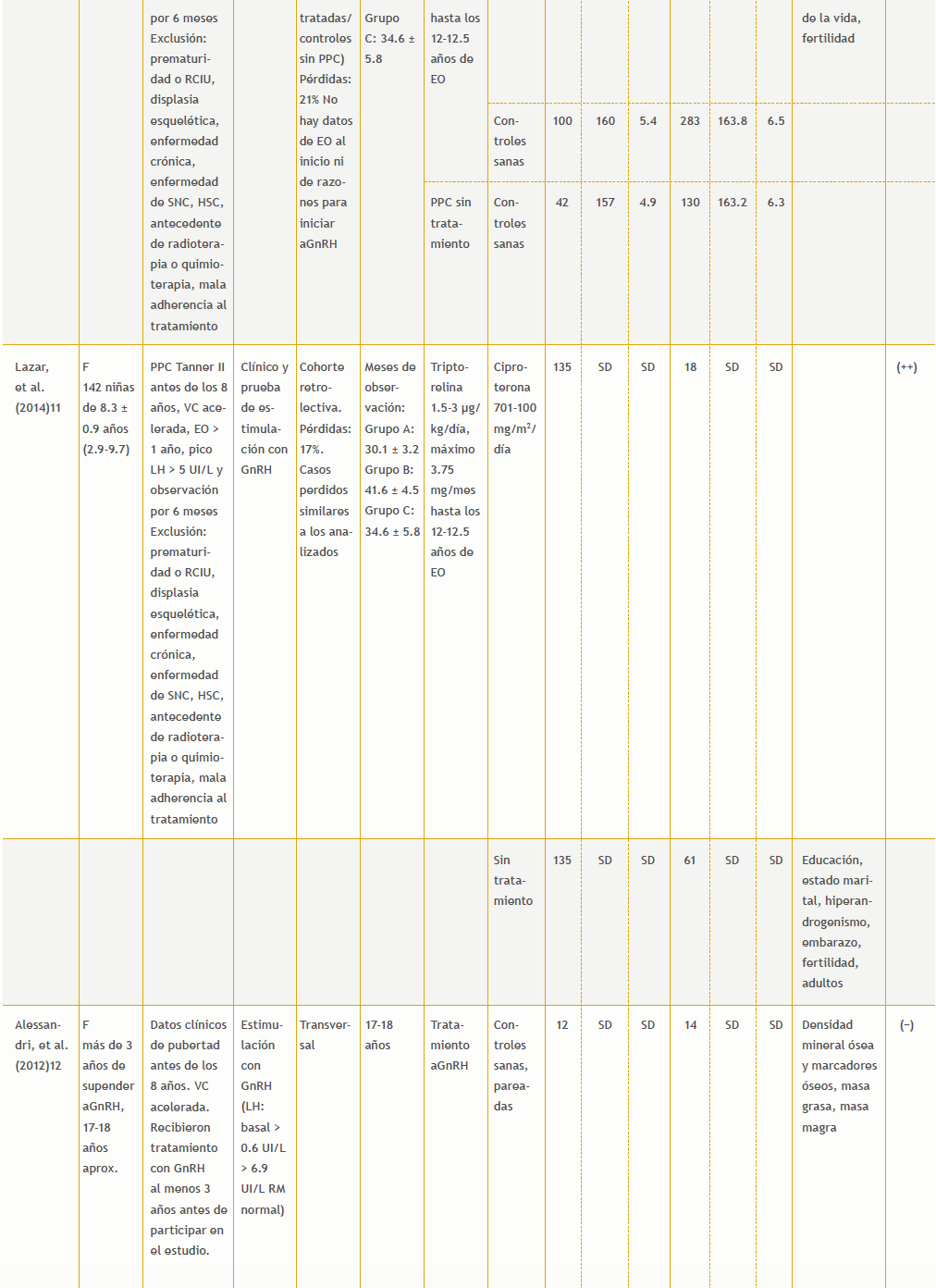
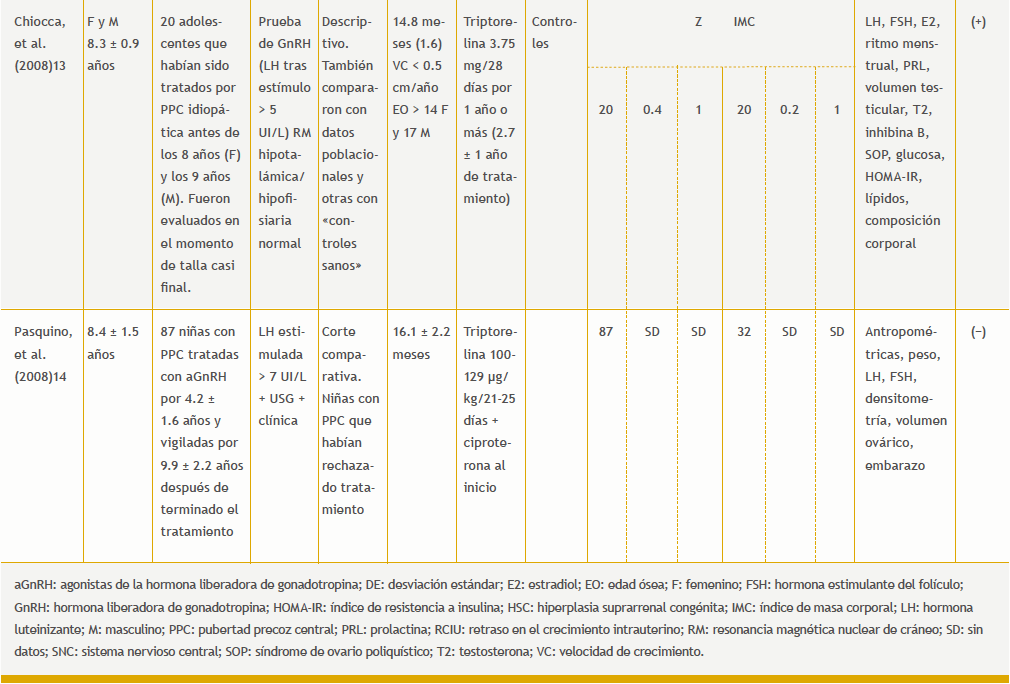
Se encontraron 104 referencias. Cinco estudios cumplieron los criterios de inclusión (Tabla 3 del anexo).
Estudios sobre desenlaces psicosociales
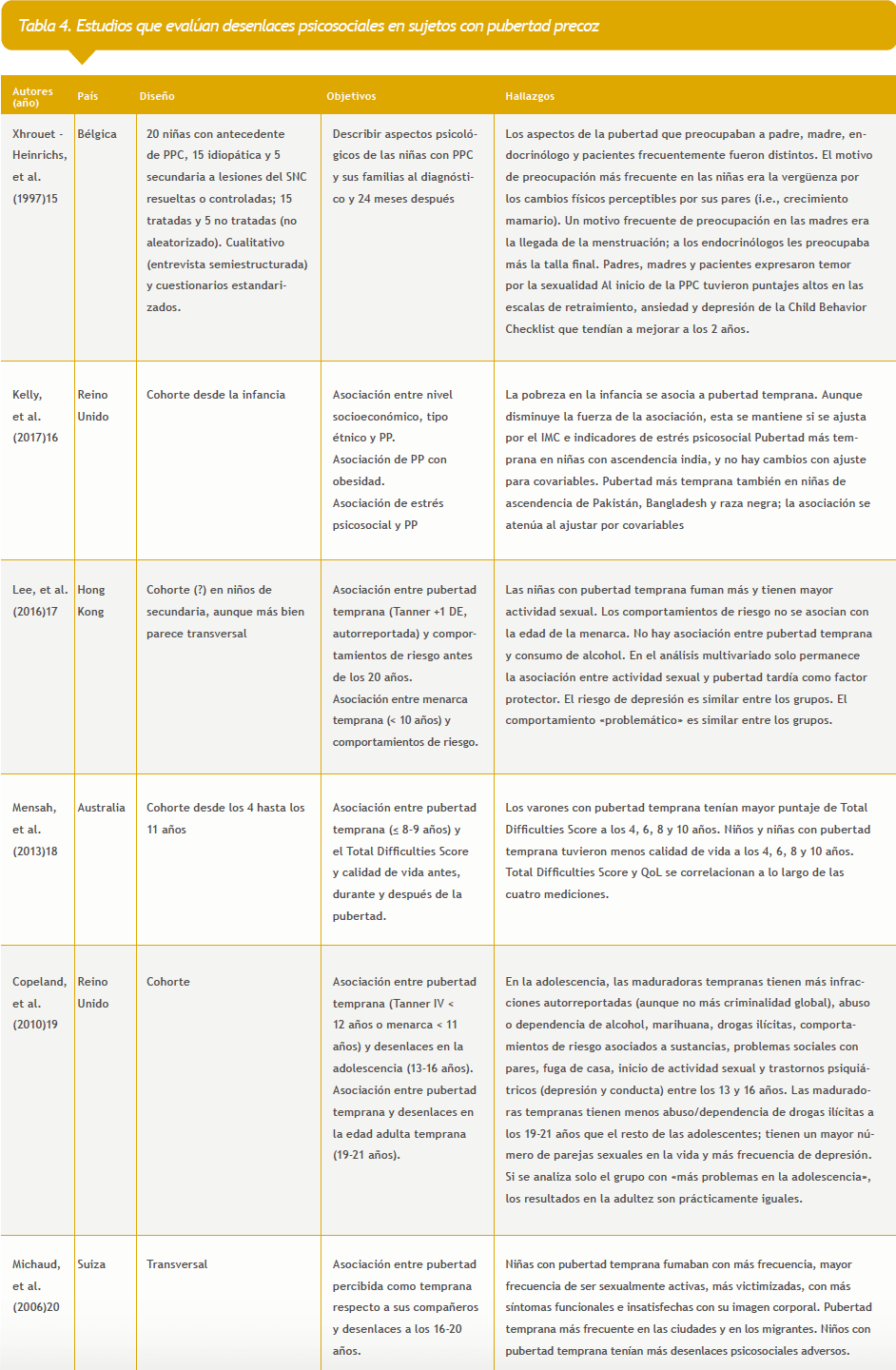
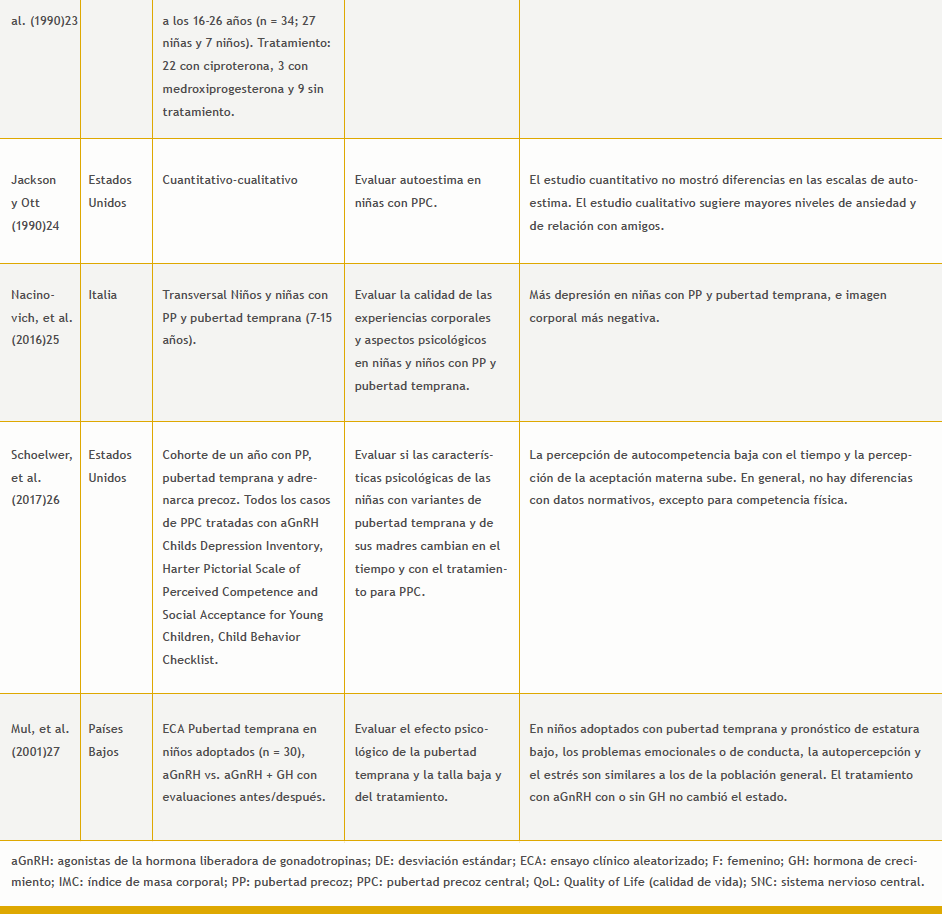
Se obtuvieron 81 referencias. En ninguno de los estudios se evaluó el efecto del bloqueo de la pubertad en los desenlaces psicosociales. La tabla 4 del anexo describe los estudios que se aproximan a la evaluación del efecto de la pubertad precoz/temprana en los desenlaces psicosociales.
Intervenciones adyuvantes en el tratamiento de la pubertad precoz
Metodología
Criterios de inclusión
– Tipo de estudios: ensayos clínicos controlados con o sin aleatorización y con o sin cegamiento.
– Tipo de participantes: niñas menores de 8 años con crecimiento mamario (estadio de Tanner II o mayor) y niños menores de 9 años con crecimiento testicular (volumen testicular de 4 cm3 o mayor).
– Intervención: cualquier intervención diferente de los aGnRH con o sin cointervenciones. Se incluyen intervenciones psicosociales, hormona de crecimiento o cualquier otra intervención que tuviera como finalidad impactar en alguno de los desenlaces de interés.
– Control: sujetos que no recibieron la intervención. Pueden ser sujetos que no recibieron ninguna intervención o que recibieron una intervención alternativa.
– Desenlaces: talla adulta o casi adulta, medidas de impacto psicológico o de calidad de vida, medidas de éxito en el bloqueo de la pubertad, medidas de salud ósea y medidas de salud metabólica.
Estrategia de búsqueda
Se realizó una búsqueda en PubMed con los términos (“precocious puberty”) AND (“treatment” OR “therapy”) NOT (“GnRH analog” OR “GnRH agonist” OR “gonadotropin releasing hormone agonist” OR “gonadotropin releasing hormone analog” OR “gonadotropin-releasing hormone agonist” OR “gonadotropin-releasing hormone analog”). Filtro: ensayos clínicos.
También se incluyeron los estudios identificados en la búsqueda de la revisión sistemática «Análogos de la GnRH para el tratamiento de la pubertad precoz» (sección anterior de este documento).
Selección de estudios
Todos los títulos y los resúmenes identificados en la búsqueda fueron evaluados por dos revisores, quienes examinaron el texto completo de todos los ensayos que potencialmente cumplían los criterios de inclusión. Se resolvieron los desacuerdos mediante discusión con un tercer revisor hasta llegar a un consenso.
Extracción de datos
Dos revisores por estudio extrajeron los datos relevantes de los estudios en un formato diseñado previamente.
Cuando hubo discordancia en la captura de datos se discutió con un tercer revisor hasta llegar a un consenso.
Evaluación de calidad de los estudios incluidos
Se evaluó el riesgo de sesgo mediante la herramienta CASPe para ensayos clínicos1. Una vez considerados los rubros evaluados por este instrumento, los miembros del grupo desarrollador de la guía asignaron niveles para la calidad (de menor a mayor): −, + y ++.
Resultados
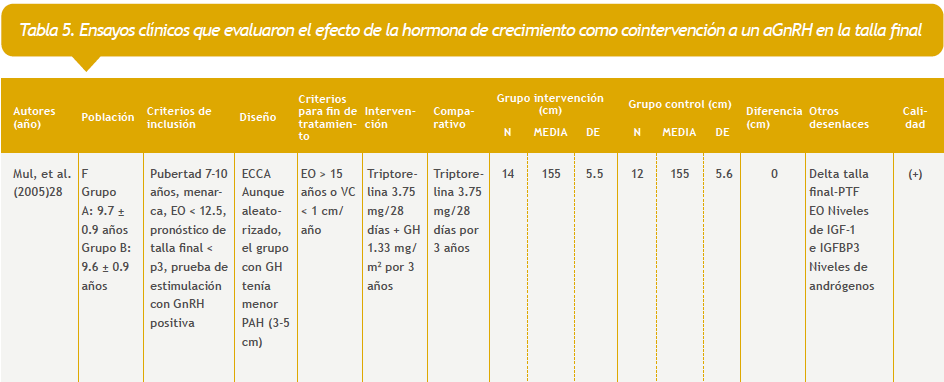
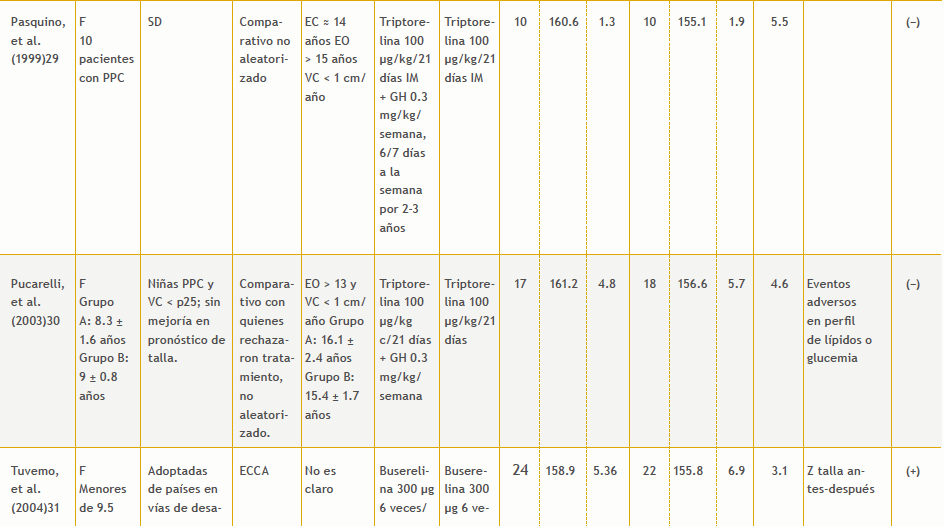
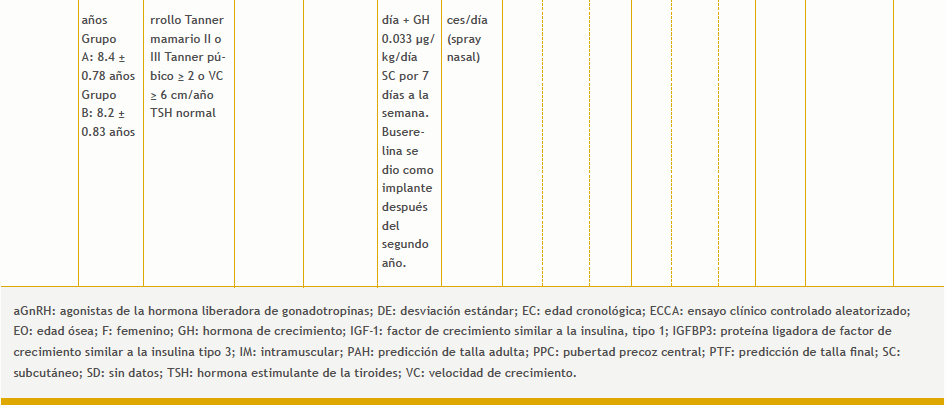
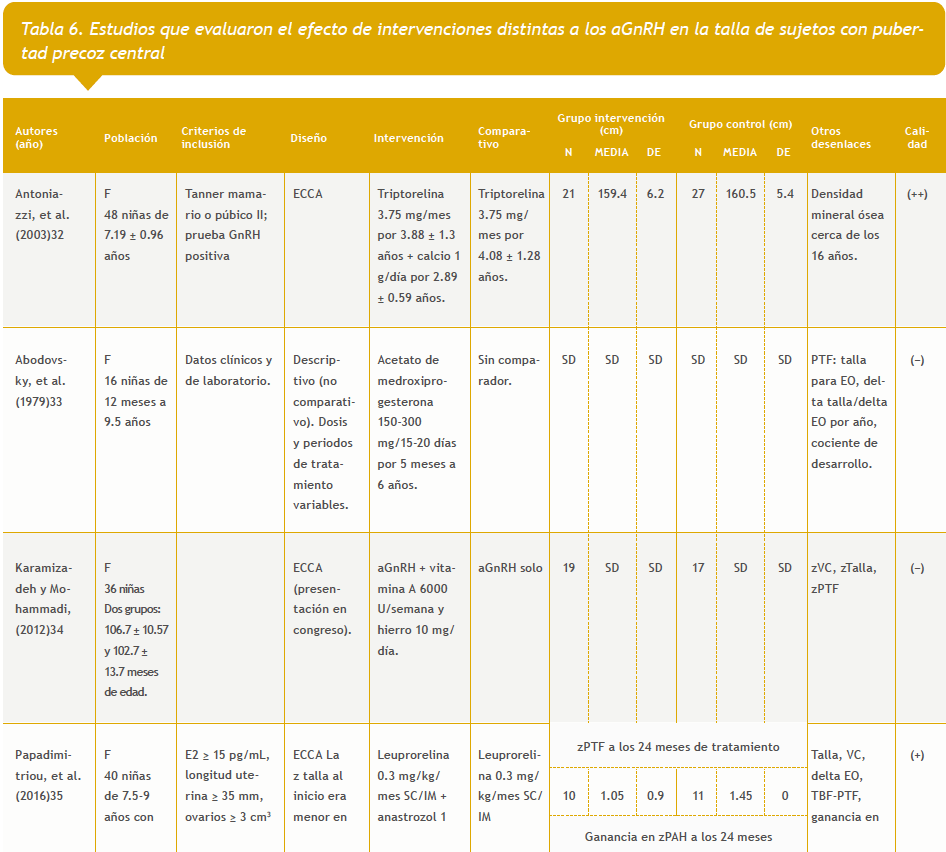
Se identificaron 140 referencias. Entre estas y las identificadas en la búsqueda para la revisión «Análogos de la GnRH para el tratamiento de la pubertad precoz», nueve estudios cumplieron los criterios de inclusión: cuatro que evaluaron el efecto de la cointervención con hormona del crecimiento en la talla final (Tabla 5 del anexo), uno que evaluó la cointervención con calcio para la densidad mineral ósea, uno que evaluó la cointervención con un inhibidor de la aromatasa, uno que evaluó la cointervención con vitamina A y con hierro, y otro que evaluó la cointervención con un antagonista de la GnRH. También se encontró un estudio comparativo que evaluó el uso de medroxiprogesterona (Tabla 6 del anexo). De los estudios con hormona del crecimiento solo se evaluaron los ensayos clínicos cuyo desenlace fuera la talla final, y no otra medida subrogada de crecimiento.
Revisión sistemática de estudios de pruebas diagnósticas para la pubertad precoz. Metodología
Criterios de inclusión
– Tipo de estudios: estudios de exactitud de pruebas diagnósticas para la pubertad de origen central.
– Tipo de participantes: niñas menores de 8 años con crecimiento mamario (estadio Tanner II o mayor) y niños menores de 9 años con crecimiento testicular (volumen testicular de 4 cm3 o mayor).
– Prueba índice: cualquier prueba con el propósito de diagnosticar la pubertad de origen central. Se incluyeron mediciones basales de hormonas, pruebas de estimulación con gonadotropinas o análogos de gonadotropinas, y mediciones ultrasonográficas.
– Pruebas de referencia (gold standard): las pruebas que se consideraron válidas como estándar fueron la progresión de la pubertad en un periodo de 6 meses (si es que esta fue definida de forma clara y precisa) y unos valores de hormona luteinizante (LH) > 5 U/l después de un estímulo con GnRH por vía intravenosa o con un aGnRH por vía subcutánea.
Estrategia de búsqueda
La búsqueda se realizó en PubMed con los términos (“precocious puberty” [Title/Abstract] OR “early puberty” [Title/Abstract]) AND (Diagnosis [Title/Abstract] OR diagnostic [Title/Abstract] OR sensitivity [Title/Abstract] OR specificity [Title/Abstract] OR “predictive value” [Title/Abstract] OR “false positive” [Title/Abstract] OR “false negative” [Title/Abstract] OR “differential diagnosis” [Title/abstract] OR “secondary causes” [Title/abstract]).
Selección de estudios
Todos los títulos y los resúmenes identificados en la búsqueda fueron evaluados por dos revisores, quienes examinaron el texto completo de todos los ensayos que potencialmente cumplían los criterios de inclusión. Se resolvieron los desacuerdos mediante discusión con un tercer revisor hasta que se llegó a un consenso.
Extracción de datos
Dos revisores por estudio extrajeron los datos relevantes de los estudios en un formato diseñado previamente.
Cuando hubo discordancia en la captura de datos se discutió con un tercer revisor hasta llegar a un consenso.
Evaluación de la calidad de los estudios incluidos
Los estudios se clasificaron en tres niveles: los de nivel 1 son los de mayor calidad, los de nivel 2 solo presentan uno de los criterios de sesgo evaluados y los de nivel 3 son aquellos con dos o más criterios de sesgo.
Resultados
Se identificaron 668 referencias en PubMed hasta el 13 de febrero de 2018, de las que se excluyeron 644 por no cumplir los criterios de inclusión. Se extrajeron los datos de 24 estudios. Algunos estudios evaluaron más de una prueba diagnóstica:
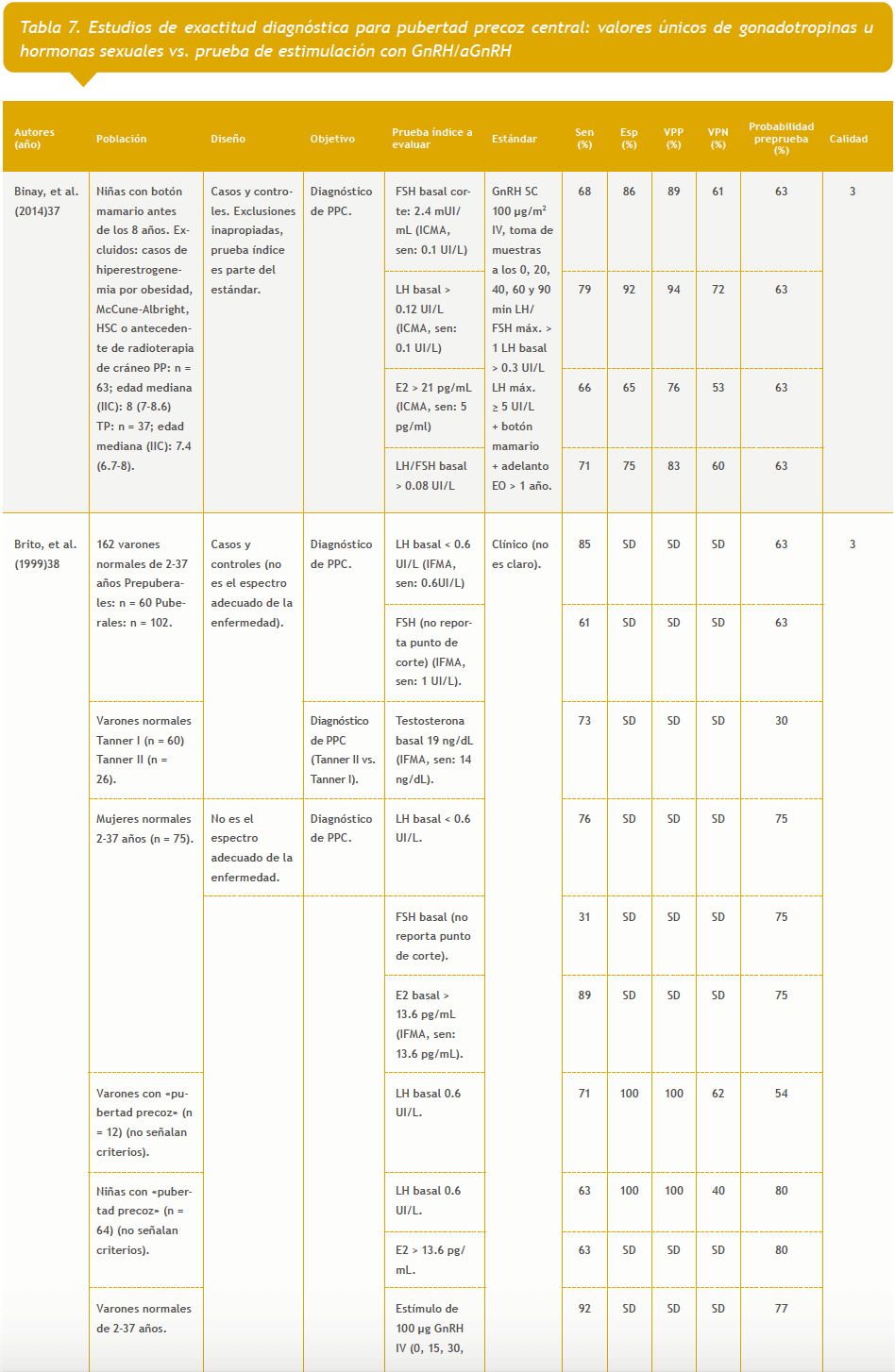
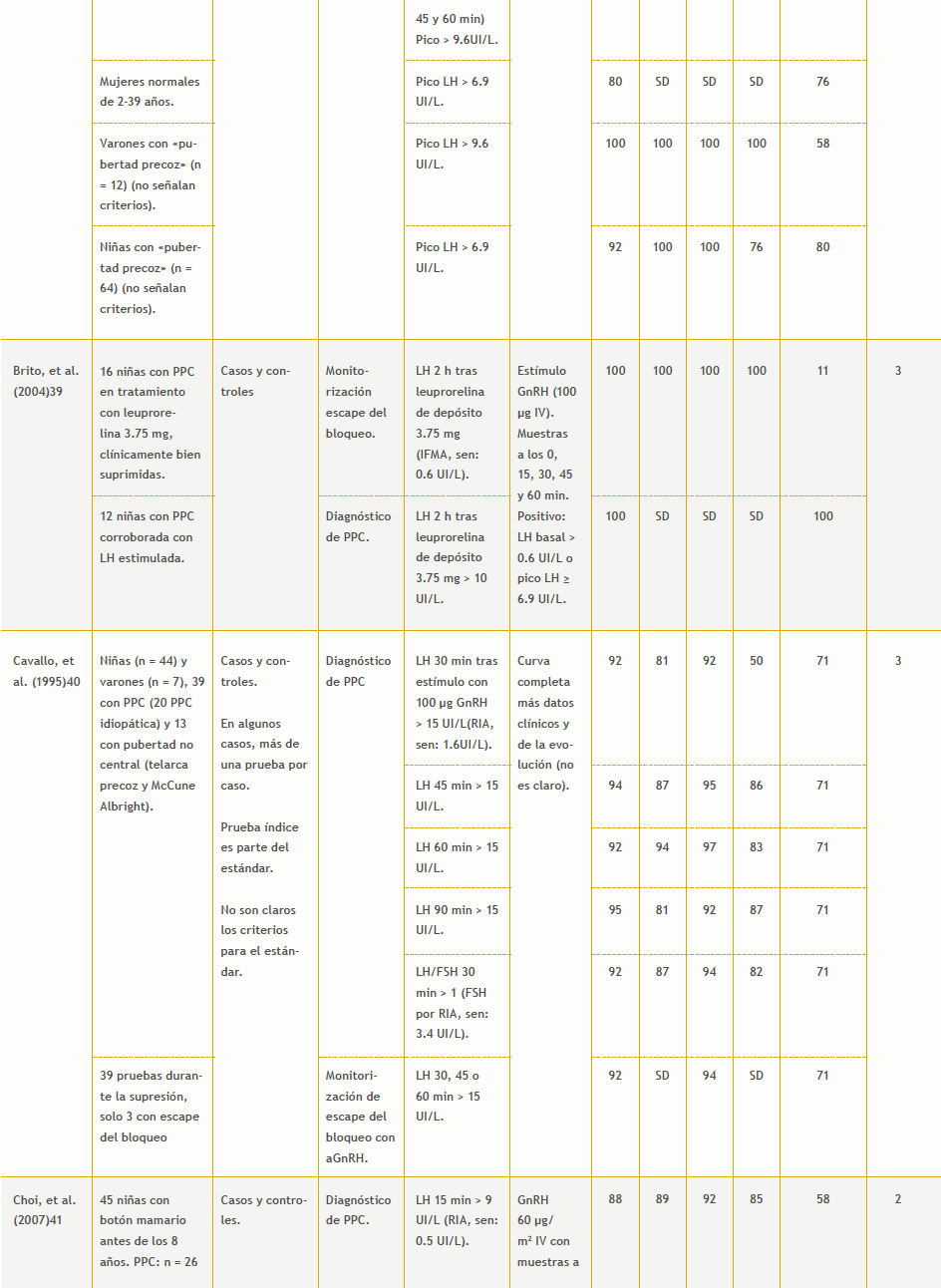
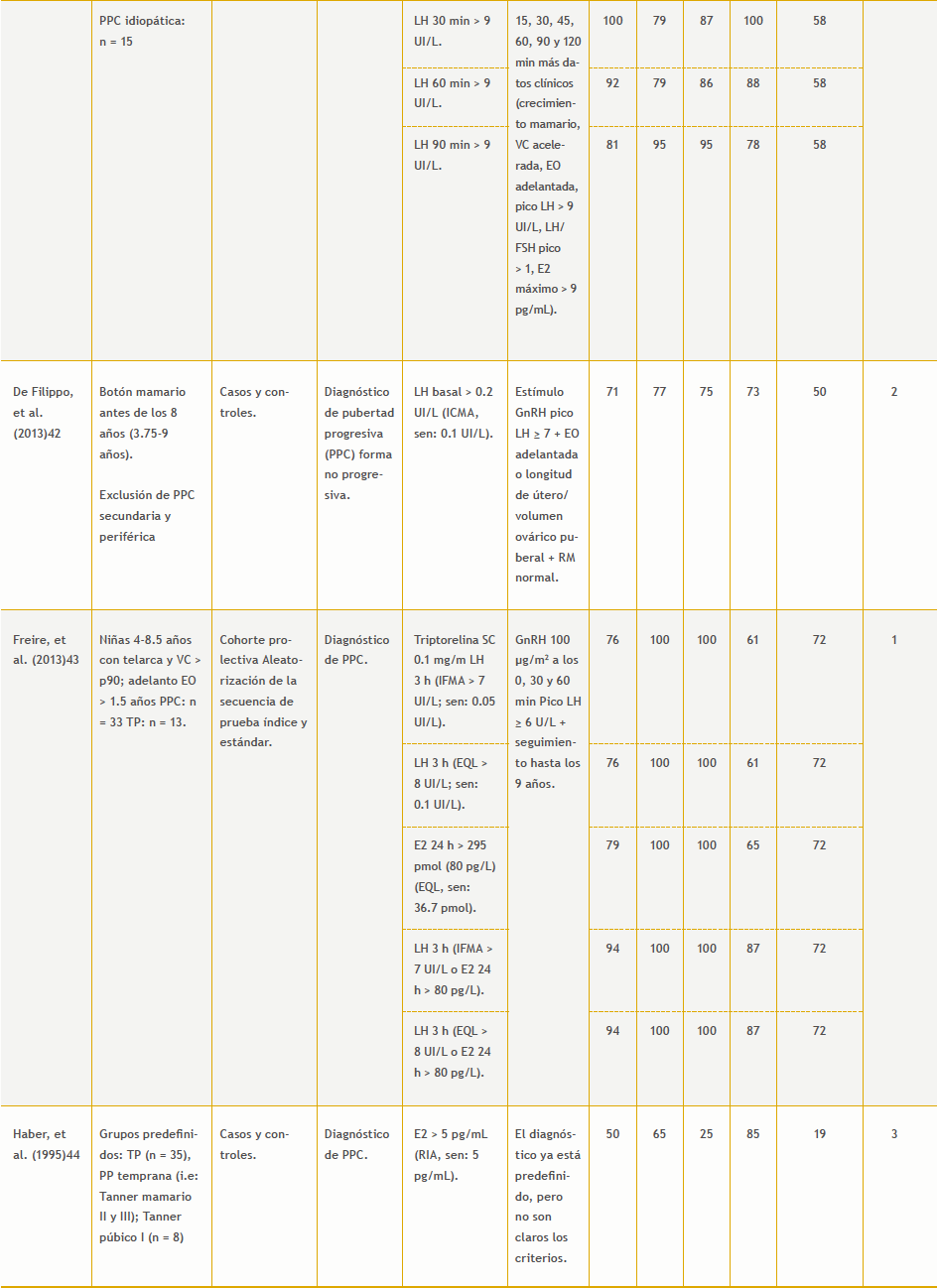
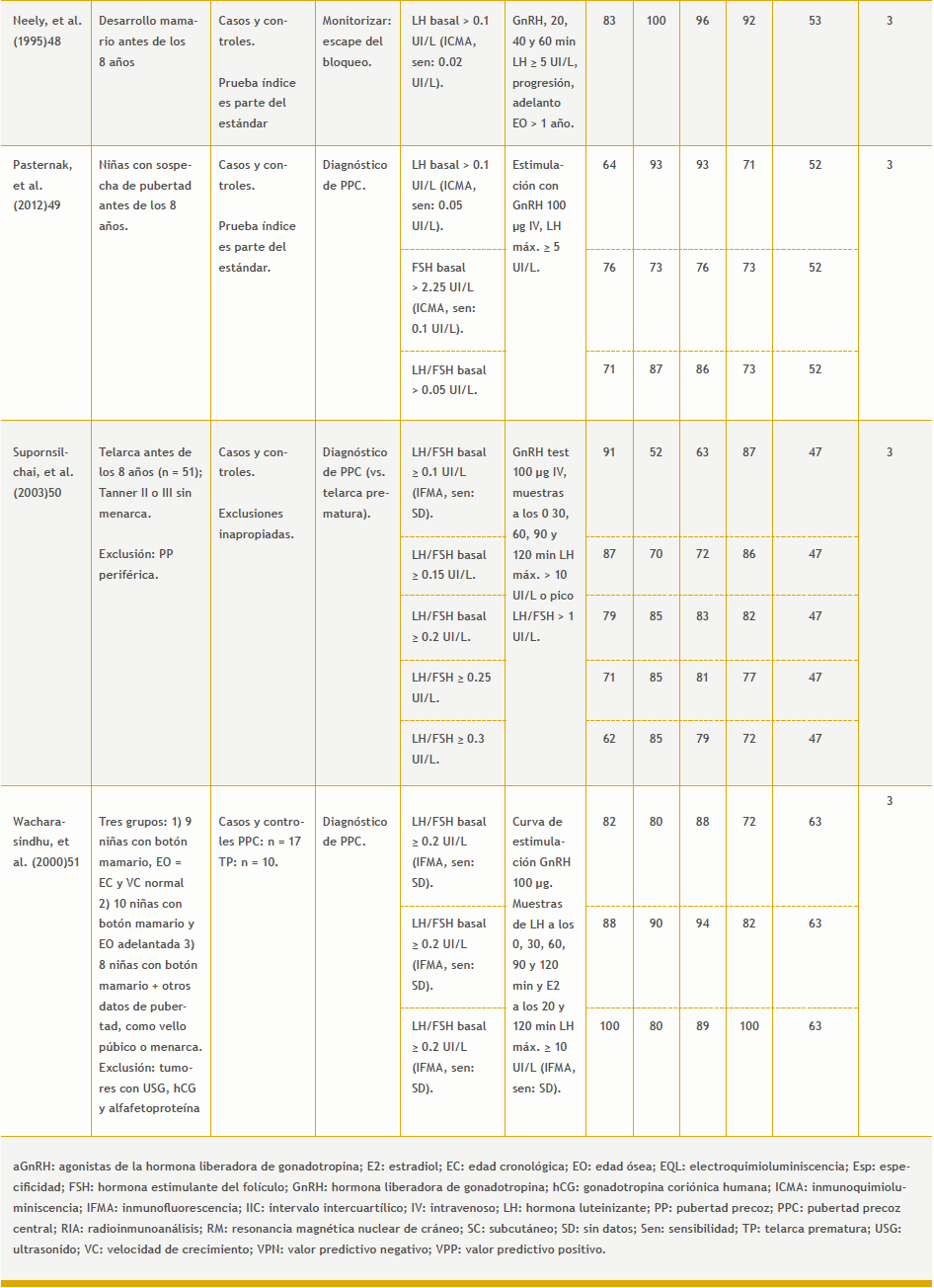
– Valores únicos de gonadotropinas u hormonas sexuales vs. prueba de estimulación con GnRH: 17 estudios (Tabla 7 del anexo).
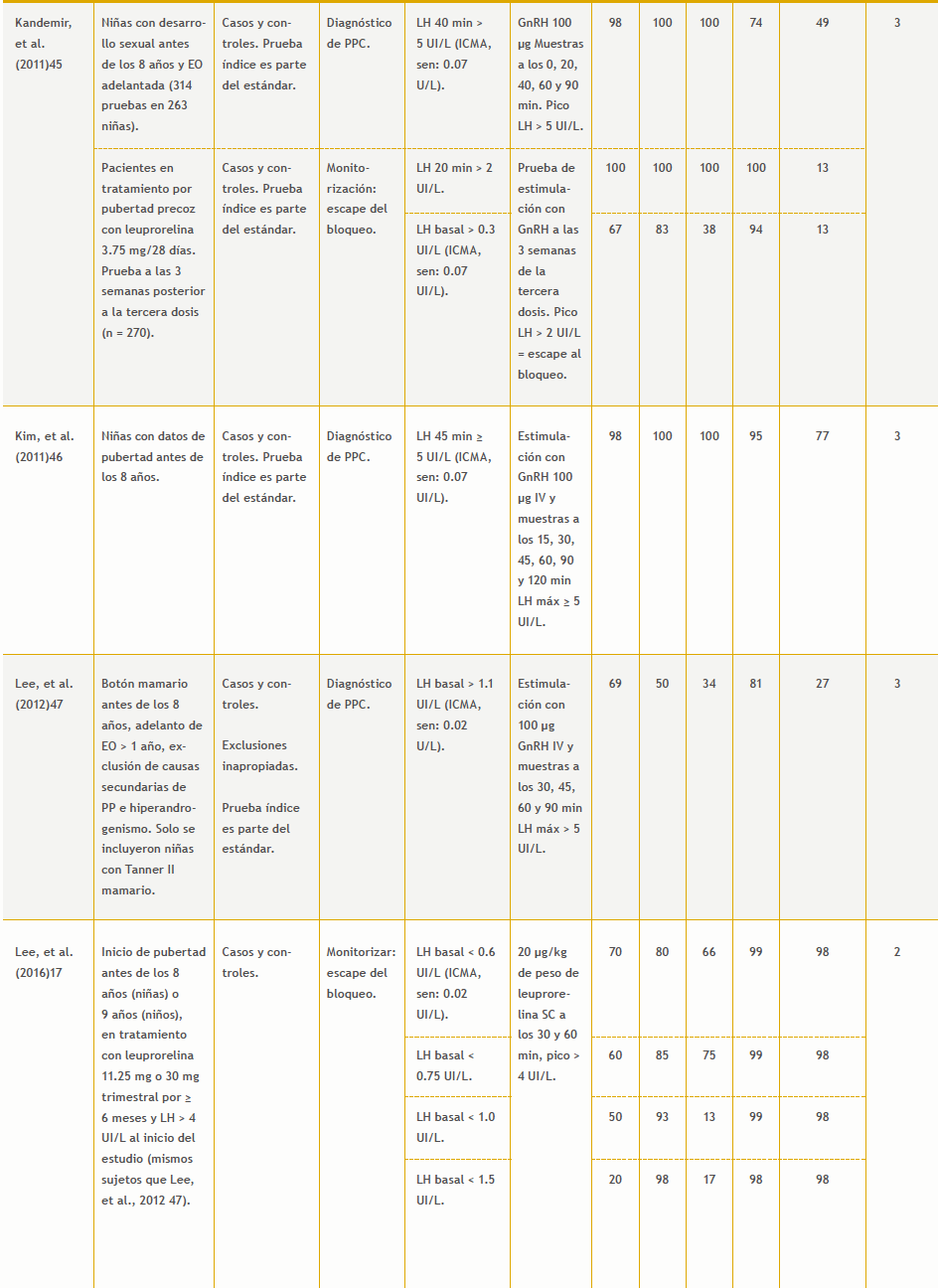
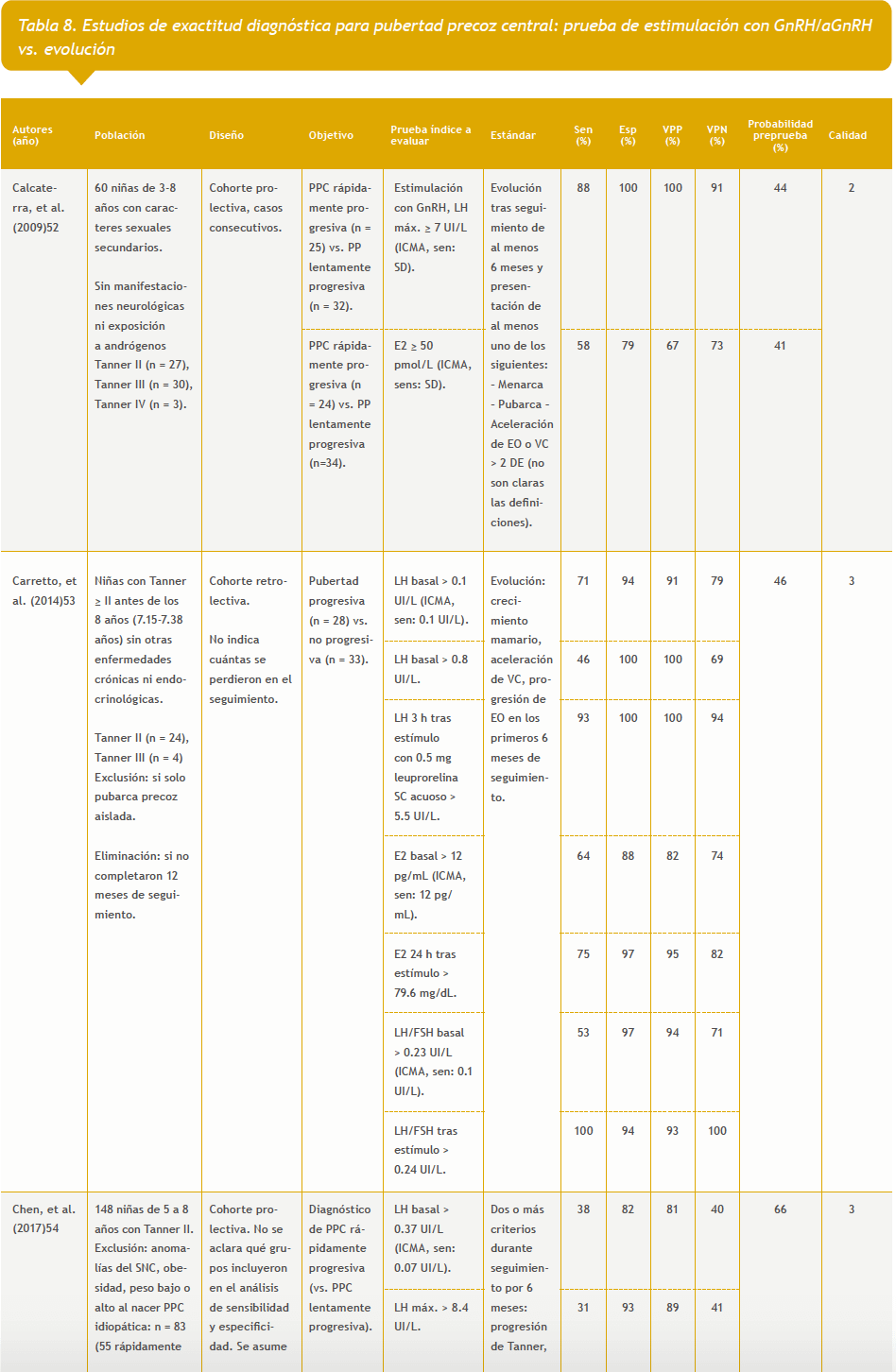
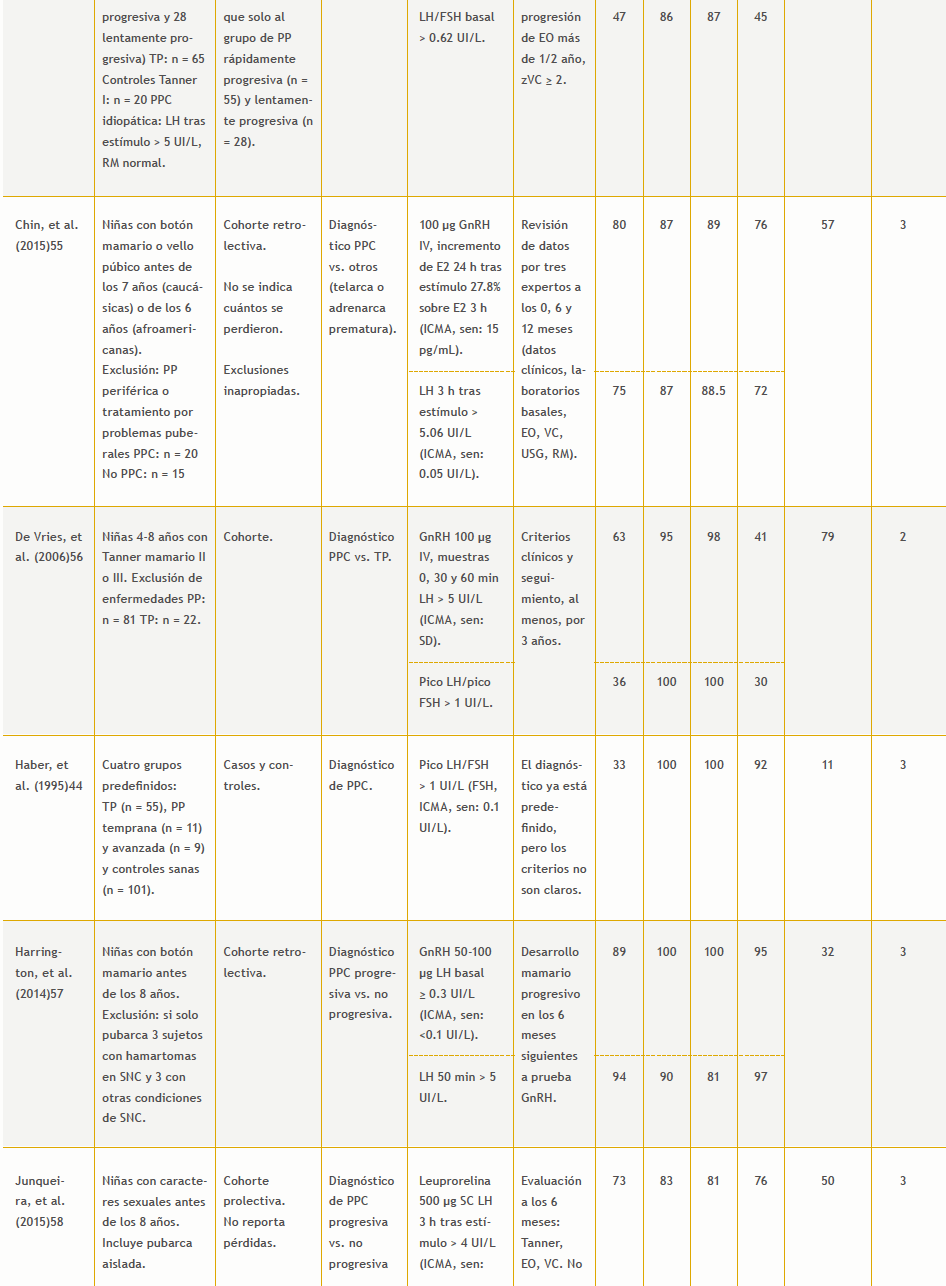
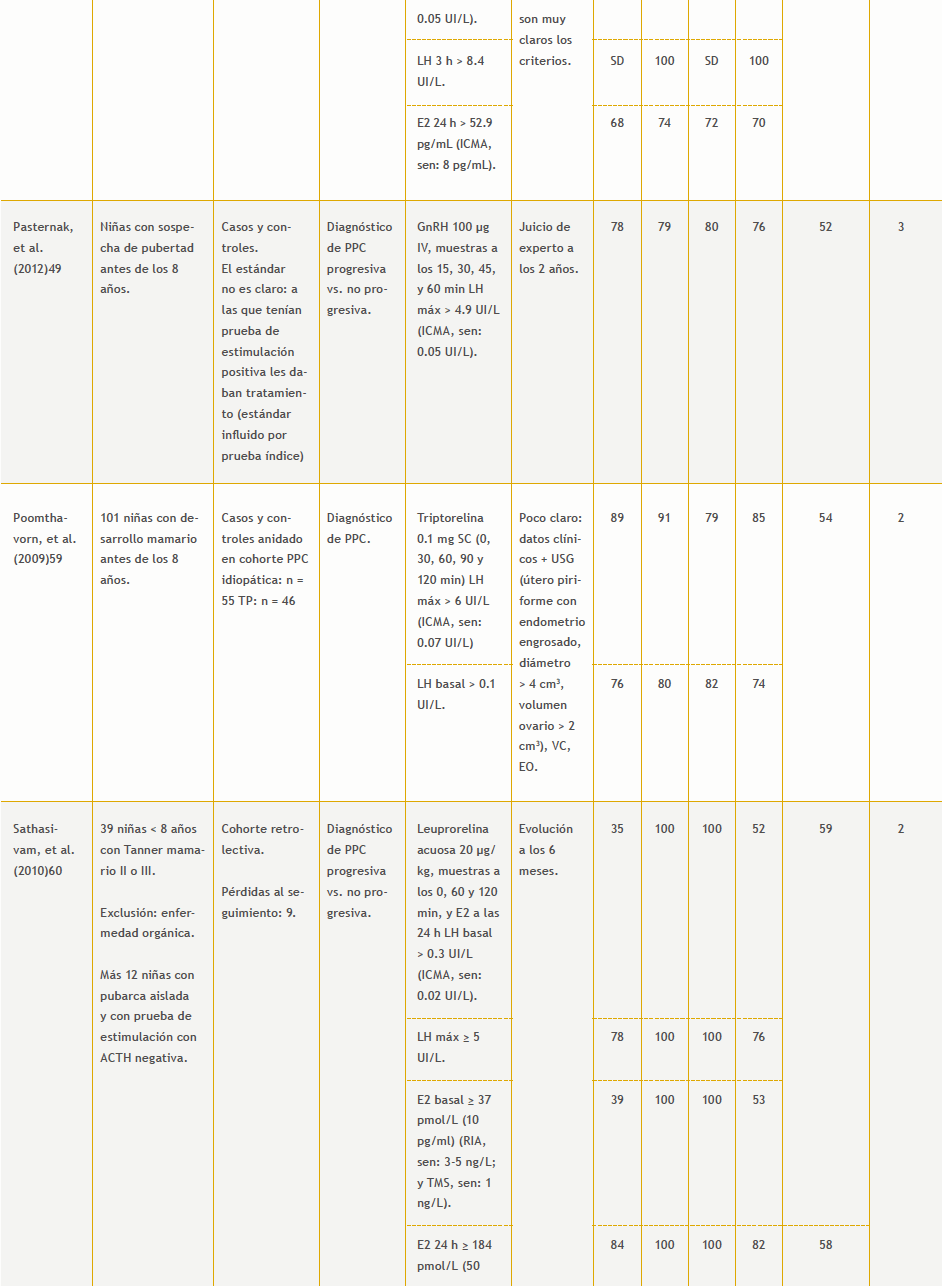
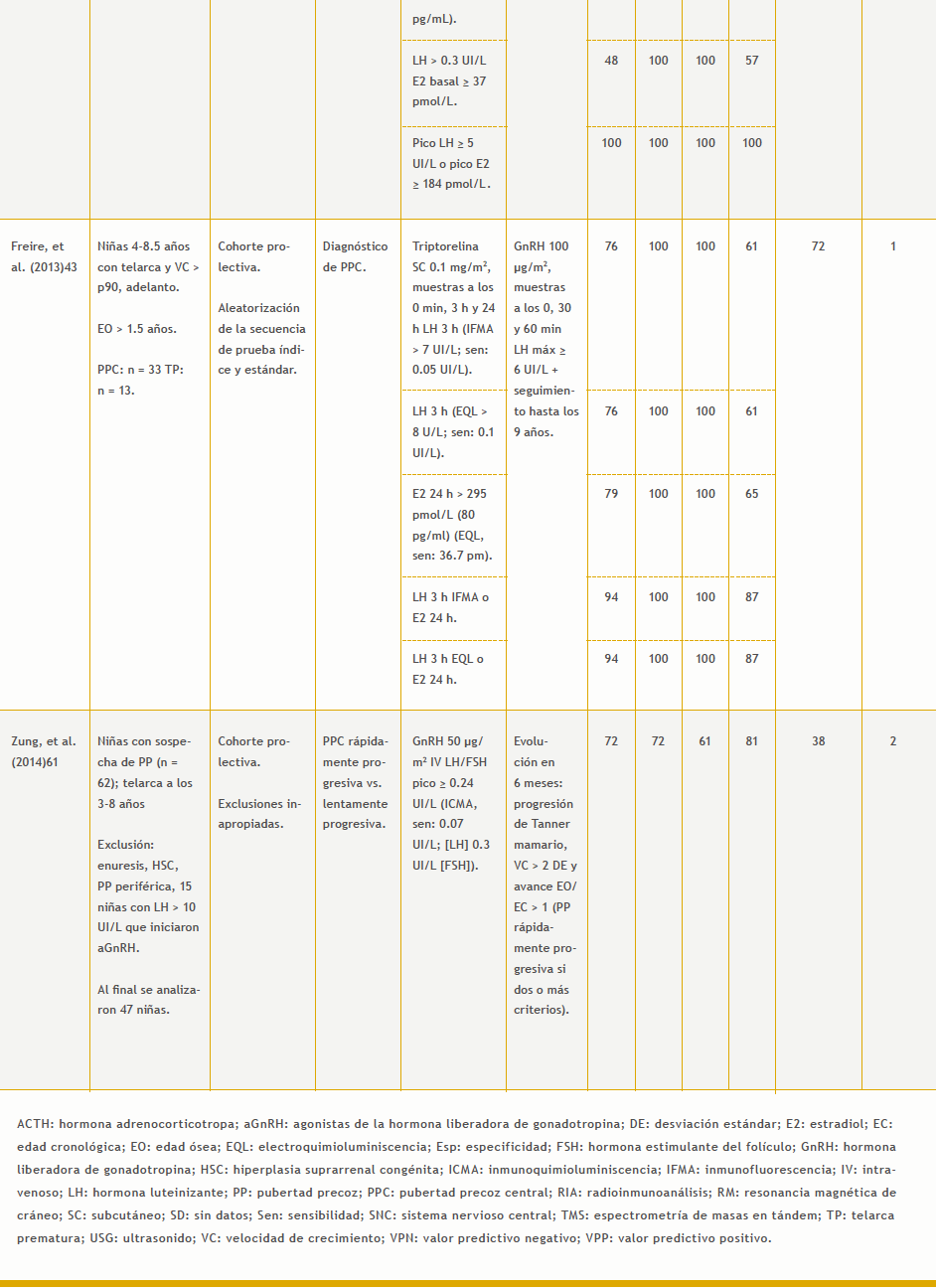
– Prueba de estimulación con GnRH vs. evolución: 12 estudios (Tabla 8 del anexo).
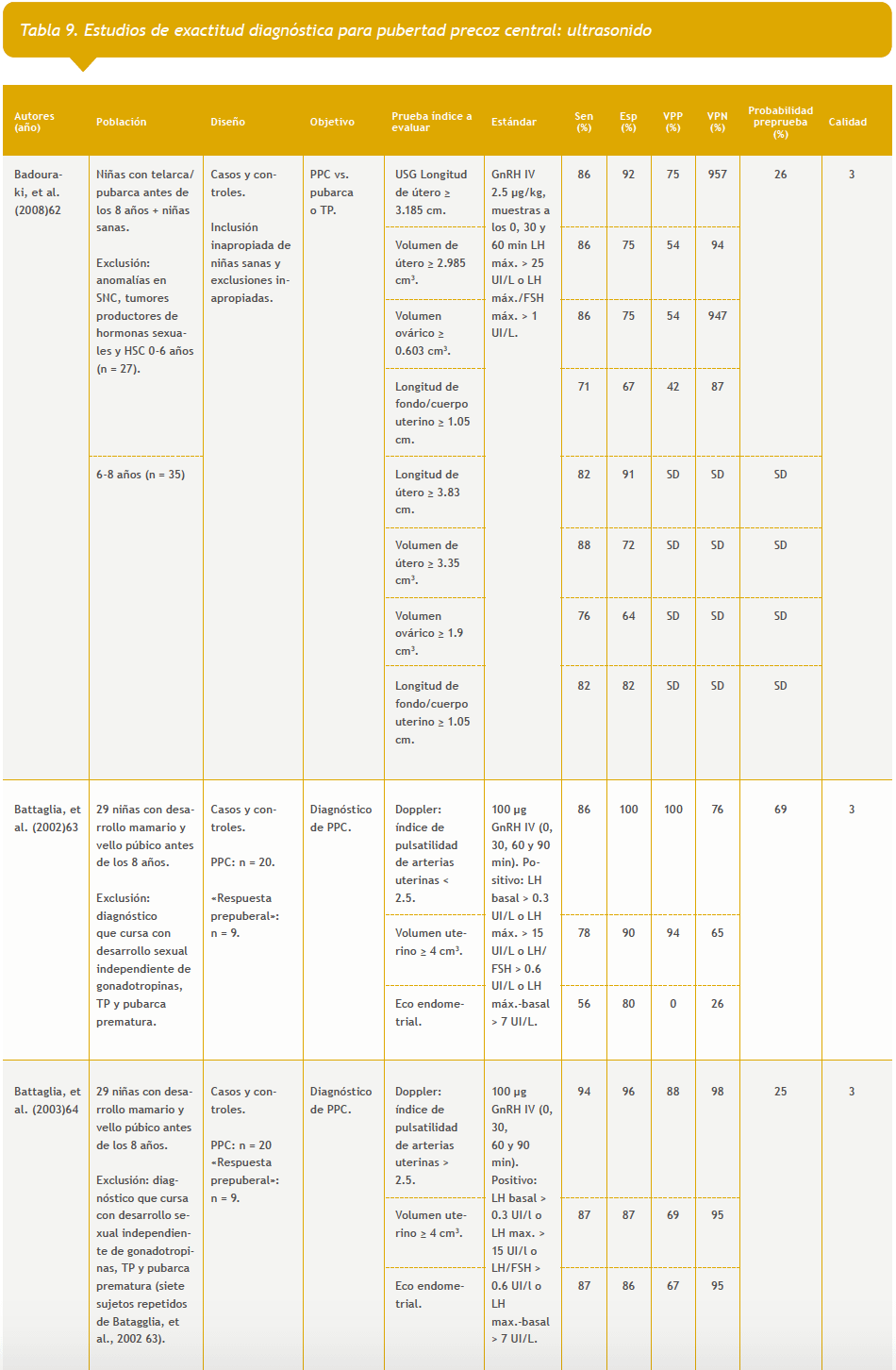
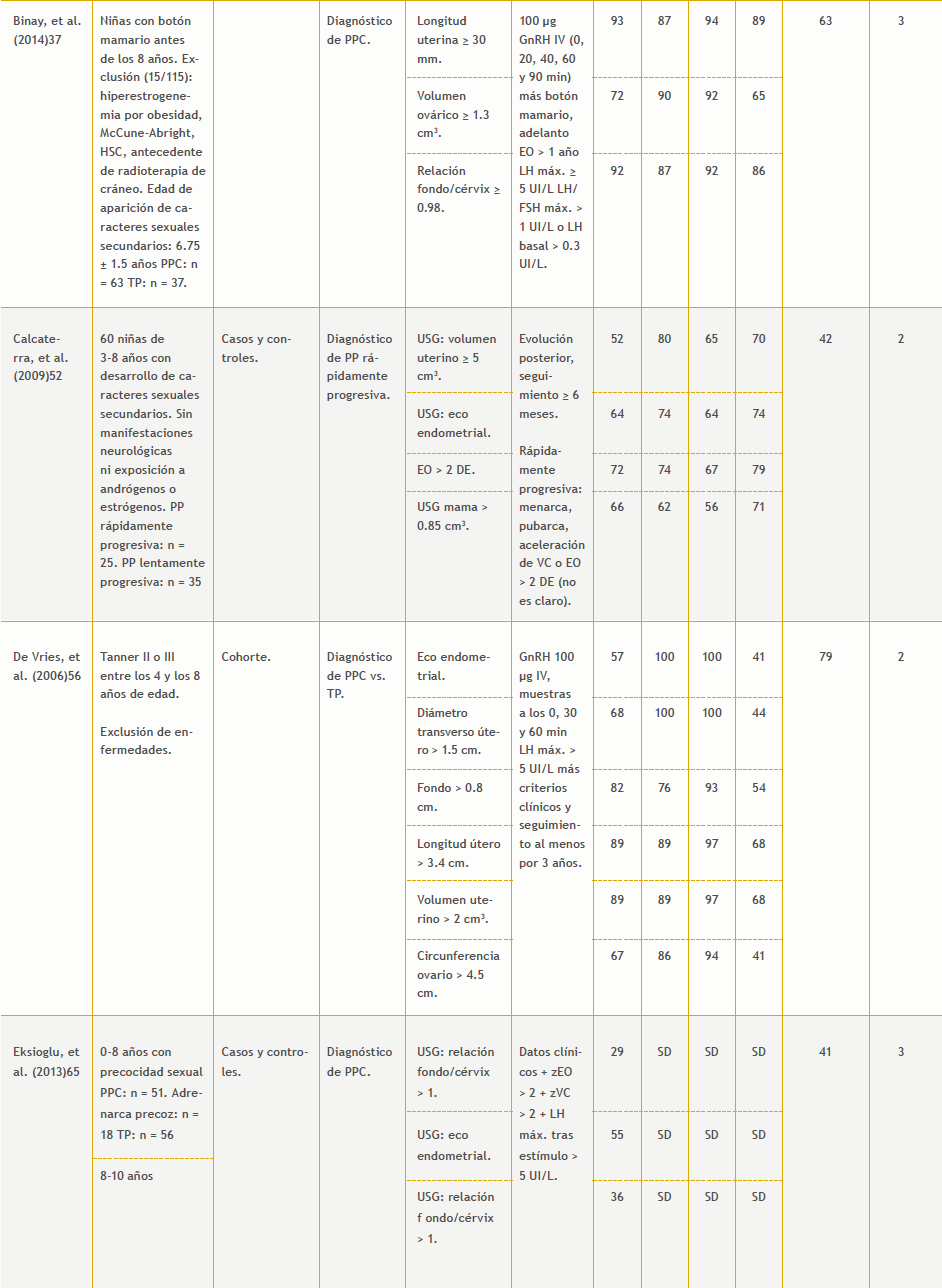
– Ultrasonido: ocho estudios (Tabla 9 del anexo).
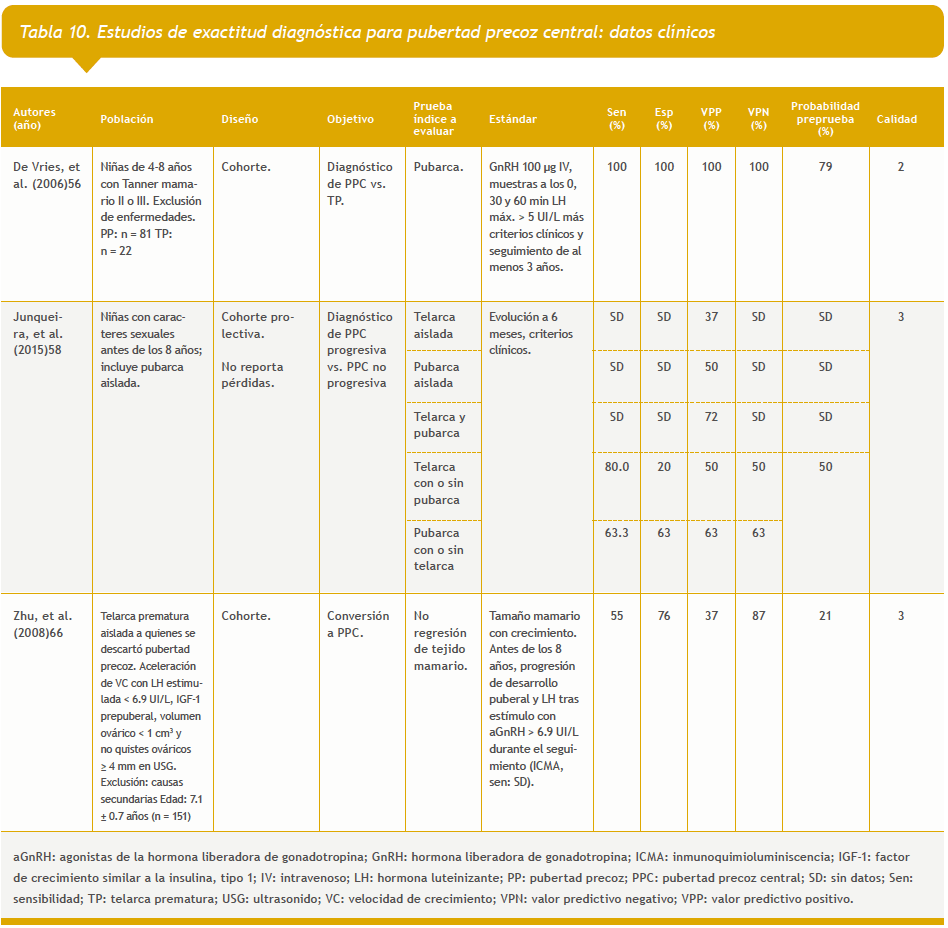
– Datos clínicos: cuatro estudios (Tabla 10 del anexo).
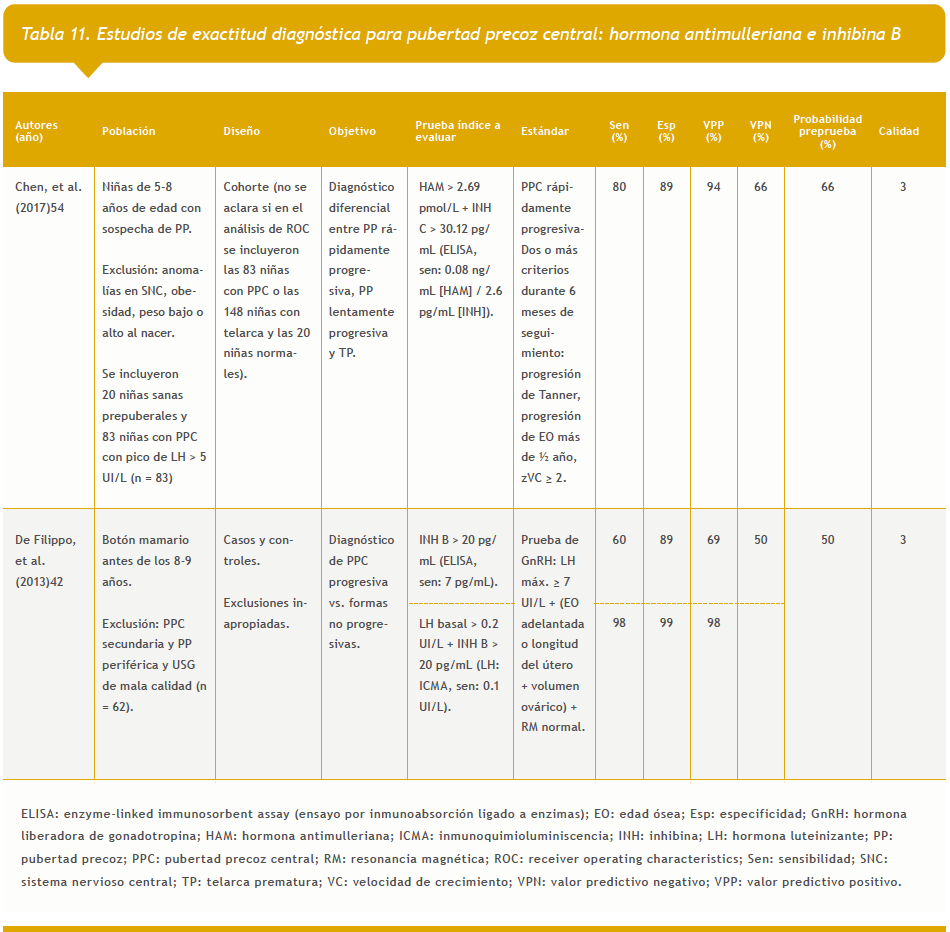
– Inhibina y hormona antimulleriana: dos estudios (Tabla 11 del anexo).
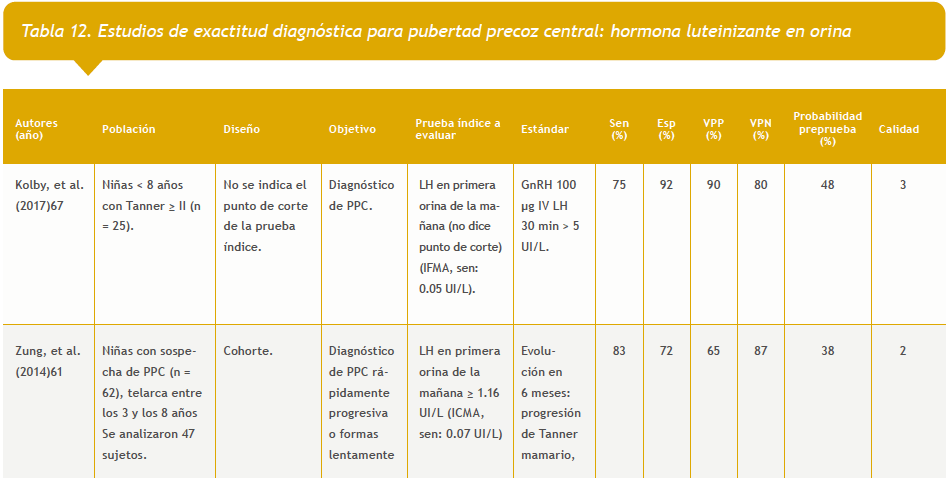
– LH matutina: dos estudios (Tabla 12 del anexo).
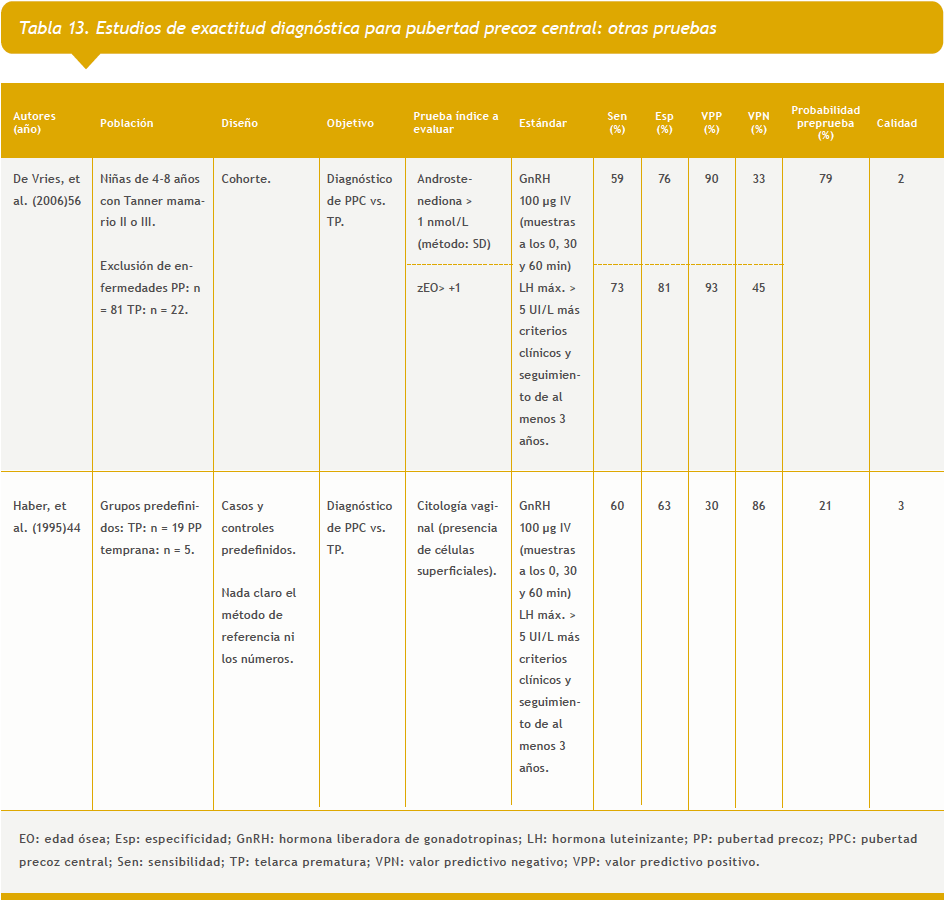
– Otras pruebas: dos estudios (Tabla 13 del anexo).
Anexo
Las tablas del anexo pueden consultarse en: www.doi.org/10.24875/BMHIM.20000087.




Referencias Bibliográficas
1. Cabello JB. Plantilla para ayudarte a entender un ensayo clínico. En: CASPe, editor. Guías CASPe de lectura crítica de la literatura médica. Cuaderno 1. Alicante: CASPe; 2005. p. 5-8.
2. Cassio A, Cacciari E, Balsamo A, Bal M, Tassinari D. Randomised trial of LHRH analogue treatment on final height in girls with onset of puberty aged 7.5-8.5 years. Arch Dis Child. 1999;81:329-32.
3. Kauli R, Galatzer A, Kornreich L, Lazar L, Pertzelan A, Laron Z. Final height of girls with central precocious puberty, untreated versus treated
with cyproterone acetate or GnRH analogue. A comparative study with re-evaluation of predictions by the Bayley-Pinneau method. Horm Res. 1997;47:54-61.
4. Sava?-Erdeve ?, ??klar Z, Hac?hamdio?lu B, Kocaay P, Çamtosun E, Öcal G, et al. Gonadotropin-releasing hormone analogue treatment in females with moderately early puberty: no effect on final height. J Clin Res Pediatr Endocrinol. 2016;8:211-7.
5. Lazar L, Kauli R, Pertzelan A, Phillip M. Gonadotropin-suppressive therapy in girls with early and fast puberty affects the pace of puberty but
not total pubertal growth or final height. J Clin Endocrinol Metab. 2002;87:2090-4.
6. Fuld K, Chi C, Neely EK. A randomized trial of 1- and 3-month depot leuprolide doses in the treatment of central precocious puberty. J Pediatr. 2011;159:982-7.e1.
7. Lee PA, Klein K, Mauras N, Neely KE, Bloch CA, Larsen L, et al. Efficacy and safety of leuprolide acetate 3-month depot 11.25 milligrams or 30 milligrams for the treatment of central precocious puberty. J Clin Endocrinol Metab. 2012;97:1572-80.
8. Mericq V, Lammoglia JJ, Unanue N, Villaroel C, Hernández MI, Ávila A, et al. Comparison of three doses of leuprolide acetate in the treatment
of central precocious puberty: preliminary results. Clin Endocrinol. 2009;71:686-90.
9. Mostafa NM, Hosmane B, Larsen LM, Chwalisz K, Chiu YL, Pradhan RS. Pharmacokinetic and exposure-response analyses of leuprolide following administration of leuprolide acetate 3-month depot formulations to children with central precocious puberty. Clin Drug Investig. 2014;34:441-8.
10. Lazar L, Lebenthal Y, Yackobovitch-Gavan M, Shalitin S, De Vries L, Phillip M, et al. Treated and untreated women with idiopathic precocious puberty: BMI evolution, metabolic outcome, and general health between third and fifth decades. J Clin Endocrinol Metab. 2015;100:1445-51.
11. Lazar L, Meyerovitch J, De Vries L, Phillip M, Lebenthal Y. Treated and untreated women with idiopathic precocious puberty: long-term follow-up and reproductive outcome between the third and fifth decades. Clin Endocrinol. 2014;80:570-6.
12. Alessandri SB, Pereira FA, Villela RA, Antonini SRR, Elias PCL, Martinelli Jr CE, et al. Bone mineral density and body composition in girls with idiopathic central precocious puberty before and after treatment with a gonadotropin-releasing hormone agonist. Clinics. 2012;67:591-6.
13. Chiocca E, Dati E, Baroncelli GI, Mora S, Parrini D, Erba P, et al. Body mass index and body composition in adolescents treated with gonadotropin- releasing hormone analogue triptorelin depot for central precocious puberty: data at near final height. Neuroendocrinology. 2009;89:441-7.
14. Pasquino AM, Pucarelli I, Accardo F, Demiraj V, Segni M, Di Nardo R. Long-term observation of 87 girls with idiopathic central precocious puberty treated with gonadotropin-releasing hormone analogs: impact on adult height, body mass index, bone mineral content, and reproductive function. J Clin Endocrinol Metab. 2008;93:190-5.
15. Xhrouet-Heinrichs D, Lagrou K, Heinrichs C, Craen M, Dooms L, Malvaux P, et al. Longitudinal study of behavioral and affective patterns in girls with central precocious puberty during long-acting triptorelin therapy. Acta Paediatr. 2008;86:808-15.
16. Kelly Y, Zilanawala A, Sacker A, Hiatt R, Viner R. Early puberty in 11-year-old girls: Millennium Cohort Study findings. Arch Dis Child. 2017;102:232-7.
17. Lee PA, Luce M, Bacher P. Monitoring treatment of central precocious puberty using basal luteinizing hormone levels and practical considerations for dosing with a 3-month leuprolide acetate formulation. J Pediatr Endocrinol Metab. 2016;29:1249-57.
18. Mensah FK, Bayer JK, Wake M, Carlin JB, Allen NB, Patton GC. Early puberty and childhood social and behavioral adjustment. J Adolesc Health. 2013;53:118-24.
19. Copeland W, Shanahan L, Miller S, Costello EJ, Angold A, Maughan B. Outcomes of early pubertal timing in young women: a prospective population-based study. Am J Psychiatr. 2010;167:1218-25.
20. Michaud PA, Suris JC, Deppen A. Gender-related psychological and behavioural correlates of pubertal timing in a national sample of Swiss adolescents. Mol Cell Endocrinol. 2006;254-255:172-8.
21. Johansson TS, Ritzén EM. Very long-term follow-up of girls with early and late menarche. Abnormalities in puberty. Endocr Dev. 2005;8:126-36.
22. Baumann DA, Landolt MA, Wetterwald R, Dubuis JM, Sizonenko PC, Werder EA. Psychological evaluation of young women after medical treatment for central precocious puberty. Horm Res. 2001;56:45-50.
23. Schoevaart CE, Drop SL, Otten BJ, Slijper FM, Degenhart HJ. Growth analysis up to final height and psychosocial adjustment of treated and untreated patients with precocious puberty. Horm Res. 1990;34:197-203.
24. Jackson PL, Ott MJ. Perceived self-esteem among children diagnosed with precocious puberty. J Pediatr Nurs. 1990;5:190-203.
25. Nacinovich R, Buzi F, Oggiano S, Rossi S, Spada S, Broggi F, et al. Body experiences and psychopathology in idiopathic central precocious and early puberty. Minerva Pediatr. 2016;68:11-8.
26. Schoelwer MJ, Donahue KL, Didrick P, Eugster EA. One-year follow-up of girls with precocious puberty and their mothers: do psychological assessments change over time or with treatment? Horm Res Paediatr. 2017;88:347-53.
27. Mul D, Oostdijk W, Waelkens JJ, Schulpen TW, Drop SL. Gonadotrophin releasing hormone agonist treatment with or without recombinant human GH in adopted children with early puberty. Clin Endocrinol (Oxf). 2001;55:121-9.
28. Mul D, Oostdijk W, Waelkens JJ, Drop SL. Final height after treatment of early puberty in short adopted girls with gonadotrophin releasing hormone agonist with or without growth hormone. Clin Endocrinol (Oxf). 2005;63:185-90.
29. Pasquino AM, Pucarelli I, Segni M, Matrunola M, Cerroni F, Cerrone F. Adult height in girls with central precocious puberty treated with gonadotropin-releasing hormone analogues and growth hormone. J Clin Endocrinol Metab. 1999;84:449-52.
30. Pucarelli I, Segni M, Ortore M, Arcadi E, Pasquino AM. Effects of combined gonadotropin-releasing hormone agonist and growth hormone therapy on adult height in precocious puberty: a further contribution. J Pediatr Endocrinol Metabol. 2003;16:1005-10.
31. Tuvemo T, Jonsson B, Gustafsson J, Albertsson-Wikland K, Aronson AS, Häger A, et al. Final height after combined growth hormone and GnRH analogue treatment in adopted girls with early puberty. Acta Paediatr. 2004;93:1456-62.
32. Antoniazzi F, Zamboni G, Bertoldo F, Lauriola S, Mengarda F, Pietrobelli A, et al. Bone mass at final height in precocious puberty after gonadotropin-releasing hormone agonist with and without calcium supplementation. J Clin Endocrinol Metabol. 2003;88:1096-101.
33. Abodovsky N, Matus de la Parra A, Vivanco X, Onetto E. [Treatment of true precocious puberty with medroxyprogesterone acetate]. Bol Med Hosp Infant Mex. 1979;36:581-97.
34. Karamizadeh Z, Mohammadi H. 661 Vitamin A and iron as an adjuvant therapy in addition of GnRH agonist in precocious puberty. Arch Dis Child. 2012;97(Suppl 2):A191.
35. Papadimitriou DT, Dermitzaki E, Papagianni M, Papaioannou G, Papaevangelou V, Papadimitriou A. Anastrozole plus leuprorelin in early maturing girls with compromised growth: the “GAIL” study. J Endocrinol Invest. 2016;39:439-46.
36. Roth CL, Brendel L, Rückert C, Hartmann K. Antagonistic and agonistic GnRH analogue treatment of precocious puberty: tracking gonadotropin concentrations in urine. Horm Res. 2005;63:257-62.
37. Binay C, Simsek E, Bal C. The correlation between GnRH stimulation testing and obstetric ultrasonographic parameters in precocious puberty. J Pediatr Endocrinol Metab. 2014;27:1193-9.
38. Brito VN, Batista MC, Borges MF, Latronico AC, Kohek MBF, Thirone ACP, et al. Diagnostic value of fluorometric assays in the evaluation of precocious puberty. J Clin Endocrinol Metab. 1999;84:3539-44.
39. Brito VN, Latronico AC, Arnhold IJP, Mendonca BB. A single luteinizing hormone determination 2 hours after depot leuprolide is useful for therapy monitoring of gonadotropin-dependent precocious puberty in girls. J Clin Endocrinol Metab. 2004;89:4338-42.
40. Cavallo A, Richards GE, Busey S, Michaels SE. A simplified gonadotrophin-releasing hormone test for precocious puberty. Clin Endocrinol. 1995;42:641-6.
41. Choi JH, Shin YL, Yoo HW. Predictive factors for organic central precocious puberty and utility of simplified gonadotropin-releasing hormone
tests. Pediatr Int. 2007;49:806-10.
42. De Filippo G, Rendina D, Nazzaro A, Lonardo F, Bouvattier C, Strazzullo P. Baseline inhibin B levels for diagnosis of central precocious puberty in girls. Horm Res Paediatr. 2013;80:207-12.
43. Freire AV, Escobar ME, Gryngarten MG, Arcari AJ, Ballerini MG, Bergadá I, et al. High diagnostic accuracy of subcutaneous triptorelin test compared with GnRH test for diagnosing central precocious puberty in girls. Clin Endocrinol (Oxf). 2013;78:398-404.
44. Haber HR, Wollmann HA, Ranke MB. Pelvic ultrasonography: early differentiation between isolated premature thelarche and central precocious puberty. Eur J Pediatr. 1995;154:182-6.
45. Kandemir N, Demirbilek H, Özön ZA, Gönç N, Alika?ifo?lu A. GnRH stimulation test in precocious puberty: single sample is adequate for
diagnosis and dose adjustment. J Clin Res Pediatr Endocrinol. 2011; 3:12-7.
46. Kim HK, Kee SJ, Seo JY, Yang EM, Chae HJ, Kim CJ. Gonadotropin-releasing hormone stimulation test for precocious puberty. Korean J Lab Med. 2011;31:244-9.
47. Lee HS, Park HK, Ko JH, Kim YJ, Hwang JS. Utility of basal luteinizing hormone levels for detecting central precocious puberty in girls. Horm Metab Res. 2012;44:851-4.
48. Neely EK, Wilson DM, Lee PA, Stene M, Hintz RL. Spontaneous serum gonadotropin concentrations in the evaluation of precocious puberty. J Pediatr. 1995;127:47-52.
49. Pasternak Y, Friger M, Loewenthal N, Haim A, Hershkovitz E. The utility of basal serum LH in prediction of central precocious puberty in girls. Eur J Endocrinol. 2012;166:295-9.
50. Supornsilchai V, Wacharasindhu S, Aroonparkmongkol S, Hiranrat P, Srivuthana S. Basal luteinizing hormone/follicle stimulating hormone ratio in diagnosis of central precocious puberty. J Med Assoc Thai. 2003;86(Suppl 2):S145-51.
51. Wacharasindhu S, Srivuthana S, Aroonparkmongkol S, Shotelersuk V. A cost-benefit of GnRH stimulation test in diagnosis of central precocious puberty (CPP). J Med Assoc Thai. 2000;83:1105-11.
52. Calcaterra V, Sampaolo P, Klersy C, Larizza D, Alfei A, Brizzi V, et al. Utility of breast ultrasonography in the diagnostic work-up of precocious puberty and proposal of a prognostic index for identifying girls with rapidly progressive central precocious puberty. Ultrasound Obstet Gynecol.
2009;33:85-91.
53. Carretto F, Salinas-Vert I, Granada-Yvern ML, Murillo-Vallés M, Gómez-Gómez C, Puig-Domingo M, et al. The usefulness of the leuprolide stimulation test as a diagnostic method of idiopathic central precocious puberty in girls. Horm Metab Res. 2014;46:959-63.
54. Chen T, Wu H, Xie R, Wang F, Chen X, Sun H, et al. Serum anti-müllerian hormone and inhibin B as potential markers for progressive central precocious puberty in girls. J Pediatr Adolesc Gynecol. 2017;30:362-6.
55. Chin VL, Cai Z, Lam L, Shah B, Zhou P. Evaluation of puberty by verifying spontaneous and stimulated gonadotropin values in girls. J Pediatr Endocrinol Metab. 2015;28:387-92.
56. de Vries L, Horev G, Schwartz M, Phillip M. Ultrasonographic and clinical parameters for early differentiation between precocious puberty and premature thelarche. Eur J Endocrinol. 2006;154:891-8.
57. Harrington J, Palmert MR, Hamilton J. Use of local data to enhance uptake of published recommendations: an example from the diagnostic
evaluation of precocious puberty. Arch Dis Child. 2014;99:15-20.
58. Junqueira FR, Lara LA, Martins WP, Ferriani RA, Rosa-E-Silva AC, de Sá MF, et al. Gonadotropin and estradiol levels after leuprolide stimulation tests in Brazilian girls with precocious puberty. J Pediatr Adolesc Gynecol. 2015;28:313-6.
59. Poomthavorn P, Khlairit P, Mahachoklertwattana P. Subcutaneous gonadotropin-releasing hormone agonist (triptorelin) test for diagnosing precocious puberty. Horm Res. 2009;72:114-9.
60. Sathasivam A, Garibaldi L, Shapiro S, Godbold J, Rapaport R. Leuprolide stimulation testing for the evaluation of early female sexual maturation. Clin Endocrinol. 2010;73:375-81.
61. Zung A, Burundukov E, Ulman M, Glaser T, Rosenberg M, Chen M, et al. The diagnostic value of first-voided urinary LH compared with GNRH-stimulated gonadotropins in differentiating slowly progressive from rapidly progressive precocious puberty in girls. Eur J Endocrinol. 2014;170:749-58.
62. Badouraki M, Christoforidis A, Economou I, Dimitriadis AS, Katzos G. Evaluation of pelvic ultrasonography in the diagnosis and differentiation of various forms of sexual precocity in girls. Ultrasound Obstet Gynecol. 2008;32:819-27.
63. Battaglia C, Regnani G, Mancini F, Iughetti L, Venturoli S, Flamigni C. Pelvic sonography and uterine artery color Doppler analysis in the diagnosis of female precocious puberty. Ultrasound Obstet Gynecol. 2002;19:386-91.
64. Battaglia C, Mancini F, Regnani G, Persico N, Iughetti L, De Aloysio D. Pelvic ultrasound and color Doppler findings in different isosexual precocities. Ultrasound Obstet Gynecol. 2003;22:277-83.
65. Eksioglu AS, Yilmaz S, Cetinkaya S, Cinar G, Yildiz YT, Aycan Z. Value of pelvic sonography in the diagnosis of various forms of precocious puberty in girls. J Clin Ultrasound. 2013;41:84-93.
66. Zhu SY, Du ML, Huang TT. An analysis of predictive factors for the conversion from premature thelarche into complete central precocious puberty. J Pediatr Endocrinol Metab. 2008;21:533-8.
67. Kolby N, Busch AS, Aksglaede L, Sørensen K, Petersen JH, Andersson AM, et al. Nocturnal urinary excretion of FSH and LH in children and adolescents with normal and early puberty. J Clin Endocrinol Metab. 2017;102:3830-8.






