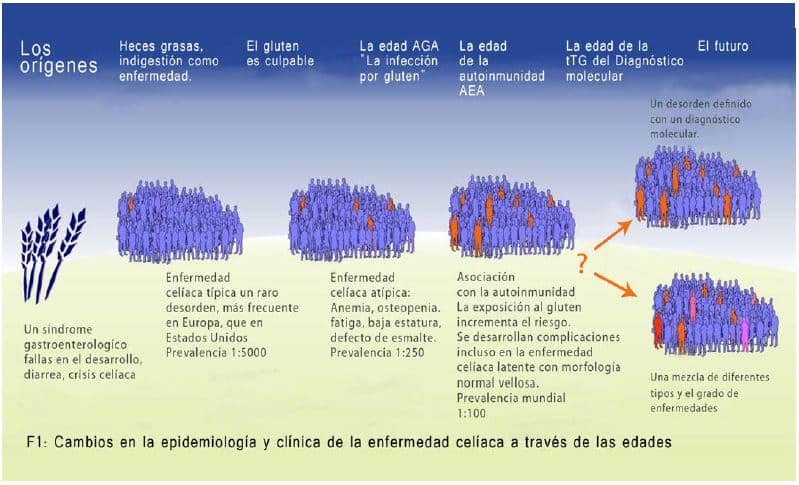
Edades de la Enfermedad Celíaca
Extractado de Alberto Tommasini, Tarcisio Not, Alessandro Ventura Publicado en la WGJ August 28, 2011 – Volume 17 – Issue 32
Las primeras descripciones de la enfermedad celiaca (EC) se refieren a un trastorno del intestino (koiliakos en griego), que se caracterizaba principalmente por heces grasas. Mientras que la diarrea era un síntoma común para una serie de enfermedades, heces grasas o esteatorrea era un síntoma poco frecuente.
El hallazgo de la esteatorrea en los niños destetados y en adultos sin fibrosis quística se describió como una sola entidad nosológica por Samuel Gee a finales del siglo 19.
Gee describe, por primera vez, que la única cura para la enfermedad sería la dieta, aunque no pudo identificar los alimentos que causaban el trastorno.
La Edad de Anticuerpos Anti-gliadina (AGA)
La enfermedad celíaca es un trastorno inmunológico La identificación de anticuerpos de gluten (AGA) en los afectados por EC revolucionó la vista de la enfermedad en 1964. La EC parecía ser debida a la respuesta inmune al gluten en lugar de a una acción directa de la proteína.
El hallazgo de anticuerpos de gluten en la EC fue aún más revolucionario, como se hizo evidente que la medición de estos anticuerpos podría permitir un diagnóstico más fácil de la enfermedad, y un cómodo seguimiento para el cambio de dieta.
Como una confirmación adicional del papel del sistema inmune en la patogénesis de EC, se observó una estrecha asociación entre el antígeno leucocitario humano (HLA) y variantes de la enfermedad. Más importante aún, la medición de la AGA, siendo un ensayo relativamente no invasivo y de bajo costo, permitió a los investigadores ampliar la búsqueda de la EC en sujetos con diferentes trastornos clínicos, y para encontrar que la enfermedad puede estar asociada con síntomas atípicos, no gastrointestinales, como la anemia, baja estatura, o la dermatitis herpetiforme.
La Edad de Anticuerpos Anti-endomisio (AEA)
La Enfermedad Celiaca está conectada a la Autoinmunidad
Como resultado del ensayo de AGA, se encontró que la EC era más común en individuos con diabetes tipo 1, y otros trastornos autoinmunes, que en la población general.
Por lo tanto, no fue sorprendente encontrar que el suero de una persona diagnosticada con EC podría contener autoanticuerpos. En la Edad de AEA, la atención se centró en la relación particular entre la EC y la autoinmunidad.
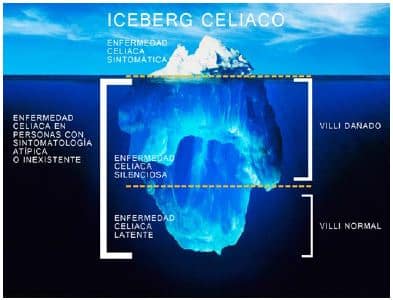
La Edad AEA culminó en la idea de que aún queda mucho que entender sobre EC, con el símil del «iceberg celíaco»: mientras que la punta está representado por los casos con síntomas típicos, la mayoría de las personas con intolerancia al gluten están bajo el agua, y son difíciles de identificar debido a los síntomas atípicos o incluso inexistentes y/o debido a la mucosa aparentemente normal. La idea del iceberg sugiere que existe un porcentaje de personas normales que pueden responder al gluten con diferentes reacciones patológicas y que las diferentes herramientas de diagnóstico podrían desentrañar la enfermedad.
La Edad AEA marcó un cambio importante en el conocimiento de la EC, un trastorno intestinal raro debido al gluten y se expresa con síntomas gastrointestinales (sólo la punta del iceberg), a un trastorno autoinmune común provocado por el gluten en el intestino. Es de destacar que la parte sumergida del iceberg es mucho más grande en comparación con la punta y, de la misma manera, los síntomas clínicos distintos del gastrointestinal son mucho más comunes que los síntomas típicos, donde la enfermedad en sí es mucho más común que lo que se consideraba anteriormente. En efecto, la EC podría ser sospechada en pacientes con una variedad de trastornos autoinmunes tales como la diabetes, la tiroiditis, la dermatitis herpetiforme, ataxia autoinmune, alopecía, así como los síntomas debidos directamente a la mala absorción.
La Edad de la Transglutaminasa
Del Objetivo a la Herramienta de Diagnóstico
Variantes HLA DQ2 y DQ8 fueron los factores genéticos que más se asocian con la EC. El aislamiento en biopsias duodenales de clones de células T que reconocen péptidos de gluten en asociación con estas moléculas de HLA confirmó aún más el papel patogénico de estas variantes genéticas.
Sin embargo, aunque este conocimiento no ha explicado por qué un paciente HLA DQ2/DQ8 puede presentar la EC y otros no. En este escenario, se espera que la identificación del antígeno, único objetivo en la reacción de tinción Endomisial que permita un mejor conocimiento de la patogénesis de la EC, y una mejor comprensión de los orígenes de la EC.
Por lo tanto, la búsqueda del «antígeno endomisial» representaba una aventura increíble para la mayoría de los investigadores que participan en la EC en la década de 1990. En 1997, Dieterich y colegas encontraron que el antígeno endomisio involucrados en la respuesta autoinmune en la EC era la enzima transglutaminasa tisular o Tipo 2 transglutaminasa (tTG o TG2). En efecto, tTG está presente en la red endomisio, donde se estabiliza el tejido conectivo por catalizar la relación entre la glutamina y la lisina de diferentes proteínas estructurales. Esta actividad es muy importante en los procesos de reparación tisular y un aumento de la actividad de la enzima puede ser evidenciado en los tejidos dañados, incluyendo la mucosa en la EC. Además, tTG juega otro papel importante, cuando grandes cantidades de gluten entran en la mucosa debido al aumento de la permeabilidad epitelial (puede ser favorecido por otros factores, tales como infecciones), la respuesta antigluten provoca daño de la mucosa, provocando la liberación y activación de tTG. El gluten en sí mismo, debido a su alto contenido en glutamina, puede ser un objetivo de tTG y puede ser entrecruzado con otras proteínas, incluyendo tTG.
Otro hallazgo de conexión tTG y el gluten se basa en la capacidad de la enzima para desaminar péptidos de gluten derivados aumentando su afinidad a la DQ2 y Dq8 HLA, empeorando así las consecuencias de la inmunidad anti-gluten. Recientemente, la medición de la respuesta inmunitaria a los péptidos de gliadina desaminados (DGP) se ha utilizado para aumentar las prestaciones del ensayo de AGA. Este modelo podría explicar en parte el papel del medio ambiente, con infecciones gastrointestinales, en la precipitación de los mecanismos patogénicos de la EC con un círculo vicioso de daño a los tejidos, la activación de tTG, la entrada y la desaminación de gluten, la respuesta antigluten y la difusión de autoanticuerpos. La hiperproducción de IL-15 se asocia con estos cambios en la mucosa, lo que podría afectar a la producción de la citoquina TGF betainmunorreguladora. Aunque este modelo no ilumina la relación específica entre la EC y otros trastornos autoinmunes, describe una inmunidad de la mucosa desregulación, que pueda interferir con los mecanismos normales de tolerancia inmunológica.
Además de contribuir al conocimiento de la patogénesis, la identificación del principal autoantígeno de la EC permitió una mejora adicional de diagnóstico basada en tTG humana recombinante (HTTG). Debido a la fiabilidad de los ensayos de HTTG, el diagnóstico de EC ahora se puede confirmar con una sola biopsia yeyunal sin ninguna necesidad de repetir los exámenes biópsicos después del inicio de la dieta. De hecho, teniendo en cuenta que se ha demostrado una fuerte correlación entre los altos niveles de anticuerpos tTG y un mayor grado de daño de la mucosa (puntuación Marsh), la ESPGHAN está evaluando la posibilidad de hacer el diagnóstico sin biopsia yeyunal de confirmación en los pacientes que tienen síntomas que pueden ser vinculados a una EC, si los anticuerpos IgA-tTG son > 10 veces el límite superior normal, AEA y HLA DQ2 y / o DQ8 son positivos.
La Edad Futura
¿Nuevas Herramientas Identificarán Nuevas Enfermedades?
Los cut-off generados por un ensayo cuantitativo tTG suponen una distribución semi-Gauss de los valores en la población sana, con una cola de altos valores que representan los pacientes celíacos verdaderos. Esto significa que los resultados positivos representan una correlación estadística del trastorno y no deben confundirse con la enfermedad en sí.
Aunque estos ensayos son muy útiles y fiables para ayudar en el diagnóstico de EC, sólo representan nuestro mejor presente, no brindan la seguridad de identificar a todos los individuos para quienes una dieta libre de gluten le podría dar ventajas mensurables. Si bien es casi seguro que muy altos títulos de anticuerpos tTG indican la presencia de la enfermedad, no es tan sencillo dar importancia a títulos bajos y a resultados border-line. De hecho, hay varias líneas que evidencian que la patología dependiente del gluten puede desarrollarse incluso en algunos pacientes con anticuerpos tTG negativos, aunque en raras ocasiones. Por otro lado, incluso algunos pacientes con tTG positivo pueden no desarrollar síntomas con una dieta que incluye gluten, aún se les debe indicar dietas libres de gluten, ya que no aún no somos capaces de predecir el riesgo de desarrollar la patología.
En efecto, la EC es un trastorno multifactorial. Simplemente podría ser que, al considerar la imagen del “iceberg celíaco», existen diferentes niveles de intolerancia al gluten, y la exposición al gluten podría tener consecuencias diferentes en cada paciente. En otras palabras, todavía conocemos sólo una parte del iceberg. La próxima Edad aclarará si seremos capaces de identificarlo como un solo trastorno por medio de los avances en el diagnóstico molecular, o si nos enfrentamos a diferentes formas de intolerancia al gluten. Recientemente, se ha argumentado que la producción intramucosa de anticuerpos anti-tTG puede preceder a su aparición en el suero y así podría representar un indicador específico de la intolerancia al gluten. Una técnica de inmunofluorescencia en biopsias yeyunales permite la detección de depósitos de IgA que la co-localizan con la tTG en el tejido conectivo velloso, que son considerados anticuerpos tTG genuinos. Estos anticuerpos podrían ser detectados en pacientes con EC latente, independientemente de su presencia en el suero, y se ha demostrado que permite predecir el desarrollo de atrofia vellosa y que desaparece durante una dieta sin gluten. Estas técnicas tienen un papel no sólo en la investigación. En la práctica clínica, los pacientes con un riesgo potencial de desarrollar enfermedades relacionados con el gluten, como los familiares de las personas diagnosticadas con EC, o con trastornos autoinmunes, pueden ser positivos para el HLA DQ2, pero tienen niveles normales de anticuerpos tTG suero.
La caracterización de tales individuos, afectados por formas intermedias o latentes de EC es uno de los objetivos de diagnósticos modernos y, una nueva clave para desentrañar un mejor conocimiento de la enfermedad.