
Bioseguridad en el laboratorio: medidas importantes para el trabajo seguro
El profesional del laboratorio de análisis clínicos, de diagnóstico o de patología clínica está siempre expuesto a la posibilidad de infectarse con muestras de patógenos altamente infecciosos. Las medidas de bioseguridad que deben tomarse en cuenta en la práctica laboral ya fueron establecidas por organismos nacionales e internacionales y deben ser seguidas a plenitud.
Humberto H. Lara-Villegas (1), Nilda Vanesa Ayala-Núñez (2), Cristina Rodríguez-Padilla (3)
(1) Laboratorio de Bioseguridad Nivel 3 del Laboratorio de Inmunología y Virología de la Facultad de Ciencias Biológicas de la Universidad Autónoma de Nuevo León
(2) Estudiante del Doctorado en Microbiología en la Facultad de Ciencias Biológicas de la Universidad Autónoma de Nuevo León
(3) Laboratorio de Inmunología y Virología de la Facultad de Ciencias Biológicas de la Universidad Autónoma de Nuevo León
Correspondencia: Dr. Humberto H. Lara Villegas. Laboratorio de Bioseguridad Nivel 3 (BSL – 3). Laboratorio de Inmunología y Virología de la Facultad de Ciencias Biológicas. Edificio “C” 3er piso, Universidad Autónoma de Nuevo León, Ave. Pedro de Alba y Manuel Barragán S/N Ciudad
Universitaria, 66451. San Nicolás de los Garza, Nuevo León, México, Fax: 83 52 42 12.
E-mail: dr.lara.v@gmail.com
Bioquimia, Volumen 33 No. 2 Abril-Junio 2008. p. 59-70
Resumen
El profesional del laboratorio de análisis clínicos, de diagnóstico o de patología clínica está siempre expuesto a la posibilidad de infectarse con muestras de patógenos altamente infecciosos. Las medidas de bioseguridad que deben tomarse en cuenta en la práctica laboral ya fueron establecidas por organismos nacionales e internacionales y deben ser seguidas a plenitud. A pesar de ello, y por falta de conocimiento del riesgo en el manejo del material contaminado, del tipo de muestra que se procesa o de las medidas de bioseguridad que se deben seguir, así como la falta de un equipo de protección adecuado, condiciones laborales inhóspitas y un incorrecto desecho del material infeccioso, se presentan accidentes de trabajo. En este artículo, el principal objetivo es dar a conocer de manera general la importancia de la bioseguridad en los laboratorios que manejen material biológico-infeccioso.
Palabras clave: Bioseguridad, grupo de riesgo, riesgo de infección, infección laboral en laboratorio, niveles de bioseguridad, prácticas laborales seguras, equipo de protección personal.
Introducción
Los profesionales del laboratorio están expuestos a una variedad de riesgos a su salud relacionados con su trabajo.
Como ejemplo, se encuentran aquéllos derivados del manejo de material infeccioso, radiación, compuestos tóxicos y químicos e inflamables. En el caso particular del material biológico- infeccioso, el peligro surge de la posibilidad de exponerse a agentes patógenos e infectarse por dicha exposición. En laboratorios de diagnóstico clínico, de investigación, industriales, de patología clínica, de producción de biológicos, de enseñanza, u otros donde se lleguen a manejar patógenos aislados o muestras que los contengan, los profesionales del laboratorio debemos prestar especial cuidado en las medidas que tomamos para prevenir un accidente. Son varias las preguntas que surgen con respecto a este tema:
¿Cuáles son los organismos asociados con mayor frecuencia con infecciones contraídas en laboratorios?
¿Cómo ocurren estas infecciones? ¿Cómo pueden ser prevenidas? ¿Qué tan efectivas son las medidas de seguridad en el laboratorio? ¿Conocemos el nivel de bioseguridad al que pertenece nuestro laboratorio? ¿Sabemos qué tan peligrosos son los patógenos con los que estamos en contacto? ¿Sabemos cómo tratar y desechar adecuadamente el material biológico-infeccioso?
Como parte de un laboratorio, deberíamos ser capaces de responder a estas preguntas.De esta necesidad de información en cuanto al concepto de bioseguridad y sus implicaciones surge el presente artículo, el cual tiene como principal objetivo dar a conocer las medidas de bioseguridad que deben tomarse en cuenta en los laboratorios que manejen agentes patógenos y materiales biológico-infecciosos. A lo largo del artículo se tocarán puntos importantes en el tema de bioseguridad como la clasificación de patógenos en grupos de riesgo, las situaciones de riesgo de contagio, los niveles de bioseguridad en los laboratorios, los accidentes laborales, el manejo de desechos biológico-infecciosos y, finalmente, se abordará lo concerniente al tema en nuestro país. En cada apartado se mencionarán las normas y regulaciones internacionales que se deben tomar en cuenta o que sirven como referencia para los aspectos mencionados. Se espera que con la información proporcionada en este artículo, una persona que labore en un laboratorio se dé cuenta de las necesidades estructurales y de reglamento de su lugar de trabajo y, pueda tomar medidas para prevenir un accidente.
Antecedentes
En 1546, Girolamo Fracastoro dio inicio a la discusión sobre la importancia de las infecciones contagiosas en su obra “On contagion”. Siglos después, la “teoría germinal de las enfermedades infecciosas” propuesta por Louis Pasteur sentó las bases para la idea del microorganismo capaz de causar una enfermedad. Posteriormente se siguió trabajando con microorganismos o con muestras infectadas, estando conscientes de que la persona que los manipulase podía infectarse al tener contacto con ellos. En consecuencia, en 1865, el Barón Joseph Lister instituyó la práctica de técnicas antisépticas y del uso de ácido carbólico como desinfectante al trabajar en el quirófano (1). Desde entonces se empezaron a delinear las medidas que se deben tomar para prevenir una infección laboral, sin embargo, no fue sino hasta mediados del Siglo XX que se establecieron, en los Estados Unidos, normas de bioseguridad para el trabajo adecuado en el laboratorio (2).
Pike y Sulkin definen infección adquirida en el laboratorio (laboratory acquired infection, LAI) como aquella que resulta de trabajo en el mismo, independientemente de si ocurre en un trabajador, o en alguna otra persona que estuvo expuesta, como resultado del trabajo de investigación o clínico con agentes infecciosos (3). En 1941 se hizo el primer estudio de casos de infecciones por prácticas laborales en Estados Unidos, reportándose 74 individuos contagiados de brucelosis (2). En 1978, cuatro estudios hechos por Pike y Sulkin incluían el resultado de un análisis de 4,079 casos reportados en Estados Unidos de personal contagiado por Brucella sp., Coxiella burnetii, virus de hepatitis B (HBV), Salmonella typhi, Francisella tularensis, Mycobacterium tuberculosis, Blastomyces dermatitidis, virus de la encefalitis equina de Venezuela, Chlamydia psittaci, Coccidioides immitis, entre otros.
Menos del 20% de los casos estuvieron asociados con accidentes laborales, siendo el 80% restante atribuido a infecciones por aerosoles en personas que trabajaban directamente con el agente en cuestión (2).
La aparición del síndrome de inmunodeficiencia adquirida (SIDA) y los nuevos brotes de tuberculosis informados en la década de los ochenta, centraron la atención en la seguridad del personal del sector salud.
Se observó que los contagios se daban en todas las áreas, incluyendo en personal de laboratorio que trabajaba con muestras de pacientes infectados (4). De hecho, el 21% de los casos documentados a nivel mundial, de infecciones ocupacionales por el virus de la inmunodeficiencia humana (VIH) ocurrieron en profesionales del laboratorio (5).
De los resultados observados por Pike en 1976, para un total de 3,921 estudios, el 58.8% de las infecciones se daban en laboratorios de investigación, el 17.3% en laboratorios de diagnóstico, el 3.4% en laboratorios de producción de biológicos, el 2.7% en laboratorios de enseñanza y el resto en laboratorios sin especificación (6,7).
Posteriormente, Harding y Byers propusieron que la incidencia de infecciones adquiridas en laboratorios era del 45% en laboratorios de diagnóstico clínico y del 51% en laboratorios de investigación (2). Jacobson y col. encontraron una incidencia de 3 infecciones por cada 1,000 empleados de laboratorio en Utah, EUA. En 1986, Vesley y Hartmann informaron de 3.5 infecciones por cada 1,000 empleados en laboratorios clínicos de hospitales en Minnesota, EUA (8). Por ello, se considera que los profesionales del laboratorio tienen hasta 10 veces más posibilidades de infectarse por algún patógeno que la población en general (9). En Estados Unidos, entre 1930 y 1999 se reportaron 2,643 casos de infecciones laborales contraídas en el laboratorio, estando encabezada la lista por las infecciones causadas por las bacterias Brucella sp. (507 casos), Coxiella burnetii (456 casos), Mycobacterium tuberculosis (417 casos) y diferentes virus de hepatitis (10).
Pike comenta que los datos publicados no representan el total real de las infecciones contraídas en el laboratorio dado que “no hay forma de llegar a un estimado exacto” (11). En la mayoría de las ocasiones, las infecciones no se reportan por no poder discernir si la infección fue o no contraída en el laboratorio, ya que se dan cuenta de la infección años después de la exposición, porque se les pide que no lo hagan, por temor a hacerlo para evitar posibles conflictos laborales, entre otros (2,11). Actualmente, en la bibliografía se encuentran publicadas las infecciones laborales como casos de estudio individuales que no reflejan a detalle el problema, como el caso del grupo de trabajadores de un laboratorio de Filadelfia, EUA infectados con el virus de la vaccinia, (12) los técnicos de laboratorio infectados con Staphylococcus aureus resistente a meticilina en Holanda (13) o, el caso de los trabajadores infectados con Salmonella serotipo enteritidis al momento de producir vacunas para aves en Maine, EUA (14).
I. Identificación de los grupos de riesgo
A raíz de lo observado en los reportes iniciales, el Centers for Disease Control and Prevention (CDC) de Estados Unidos, publicó en 1974 el texto titulado “Classification of etiologic agents on the basis of hazard”, en el cual se proponía la clasificación de los agentes patógenos en cuatro grupos de riesgo (2). Posteriormente, tanto los National Institutes of Health (NIH) de los Estados Unidos como la Organización Mundial de la Salud (OMS) actualizaron el sistema, sentando así las bases para la clasificación de los laboratorios en función del grupo de riesgo al que pertenecen lospatógenos que manejan (2). Los factores utilizados para agrupar a los microorganismos son (i) patogenicidad, (ii) dosis infectiva, (iii) modo de transmisión, (iv) rango de hospedero, (v) disponibilidad de medidas de prevención efectivas y, (vi) disponibilidad de tratamiento efectivo (15). Actualmente, la clasificación es la siguiente (16):
• Grupo de riesgo 1 (GR1): Agentes no asociados con enfermedades en humanos adultos saludables ni en animales (nulo o bajo riesgo al individuo o la comunidad). Ejemplo: Bacillus subtilis, Bacillus licheniformis, ciertas cepas de Escherichia coli.
• Grupo de riesgo 2 (GR2): Agentes asociados con enfermedades humanas raramente serias para las cuales siempre hay medidas preventivas y/o terapéuticas disponibles. El riesgo de diseminación de la infección es limitado (riesgo individual moderado, bajo riesgo a la comunidad). Ejemplo: Campylobacter jejuni, Helicobacter pylori, Neisseria gonorrhoeae, Blastomyces dermatitidis, Coccidia, Toxoplasma gondii, Adenovirus, Papovavirus.
• Grupo de riesgo 3 (GR3): Agentes asociados con enfermedades humanas serias o letales para las cuales podrían estar disponibles medidas preventivas y/o terapéuticas. El contagio entre individuos infectados es poco común (alto riesgo individual, bajo riesgo a la comunidad). Ejemplo: Coxiella burnetii, Mycobacterium tuberculosis, VIH, virus de la fiebre amarilla, virus del oeste del Nilo, bacterias multirresistentes como Staphylococcus aureus resistente a meticilina (MRSA) y Streptococcus pyogenes resistente a eritromicina (SPRE).
• Grupo de riesgo 4 (GR4): Agentes causantes de enfermedades humanas serias o letales para las cuales no hay medidas preventivas y/o terapéuticas disponibles. El contagio entre individuos infectados se da fácilmente (alto riesgo individual, alto riesgo a la comunidad). Ejemplo: virus del Ébola, Marburg, Lassa.
Esta clasificación en grupos de riesgo ha sido la más utilizada desde entonces para hacer referencia a la peligrosidad de los distintos patógenos capaces de infectar al ser humano. Sin embargo, no fue hasta la publicación del texto “Biosafety in microbiological and biomedical laboratories (BMBL)” en 1984 por parte del CDC que fue posible definir con claridad los parámetros adecuados para la manipulación de estos patógenos en el laboratorio según su grupo de riesgo, dado que el sistema de grupo de riesgo no toma en cuenta dichos procedimientos.
Actualmente existen nuevas ediciones del citado texto que se recomienda revisar para profundizar en el tema (la última edición es del 2007, disponible en la página web http://www.cdc.gov/od/ohs/ (2,15). El listado de microorganismos que corresponden a cada grupo de riesgo se mantiene en constante actualización, la cual se puede verificar en la página de Internet del CDC.
Al contrario de lo que comúnmente se piensa, el manejo de patógenos pertenecientes al GR3 es común en los laboratorios del sector salud. Entre 1979 y 1999, las diez infecciones laborales más comunes que Estados Unidos fueron en su mayoría por microorganismos de este tipo (Cuadro ver a la derecha) (7).
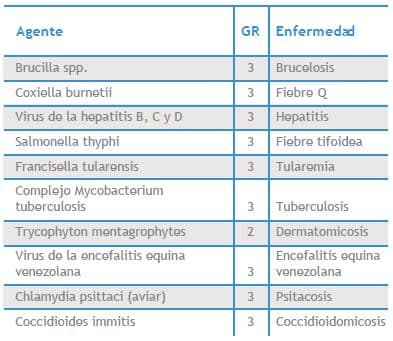
Cuadro I. Diez principales agentes biológicos causantes de infecciones laborales en el laboratorio, grupo de riesgo (GR) al que pertenecen y enfermedad que causan 6
II. ¿Cómo ocurre el riesgo de adquirir una infección en el laboratorio?
Lo observado en los informes de las infecciones laborales indica claramente cuáles fueron las vías más comunes de exposición (2,16).
Ingestión
- Pipeteo con boca.
- Salpicaduras en boca.
- Colocación en boca de artículos o dedos contaminados.
- Consumo de comida en lugar de trabajo.
Inoculación:
- Accidentes con agujas.
- Cortaduras con objetos punzo cortantes.
- Mordedura de animales.
Contaminación de piel o mucosas:
- Contacto con superficies, equipo o artículos contaminados.
- Salpicaduras en piel intacta o no intacta (con algún tipo de lesión).
- Salpicaduras en ojos, boca o nariz.
Inhalación:
- Por diversos procedimientos que producen aerosoles.
De todas ellas, la generación de aerosoles, junto con los accidentes con agujas, es una de las principales causas de infecciones adquiridas en el laboratorio. Los procedimientos más comunes que producen aerosoles son: centrifugar, moler, mezclar, agitar vigorosamente, sonicar, abrir contenedores de material infeccioso cuya presión interna pueda ser distinta a la ambiental, inocular animales por vía intranasal, colectar tejidos infectados de animales o huevos (3). La mejor forma de prevenir un accidente por exposición a aerosoles es mediante la aplicación de una técnica laboral adecuada. Para el pipeteo de muestras con Bacillus subtilis, por ejemplo, se ha estimado que la dosis de exposición por aerosol utilizando una buena técnica es de 25 microorganismos y con una técnica deficiente es de 1,200 microorganismos (10).
Aunado al tipo de ruta de inoculación, para lograr una infección viable se requiere la exposición a una dosis infectiva específica, la cual está en función del patógeno en cuestión. Por ejemplo, la dosis de Escherichia coli O157: H7 es de 10 UFC vía oral, de Campylobacter jjuni es alrededor de 500 UFC vía oral, de Francisella tularensis es 10 UFC vía nasal, de Bacillus anthracis es de 83 a 503 UFC vía nasal, de Mycobacterium tuberculosis y Boris es menor a 10 UFC vía nasal, de Poliovirus es 2 UFP vía oral (7,17). III.
III. Niveles de bioseguridad en los laboratorios
A partir de la definición de los grupos de riesgo se generó la clasificación de los laboratorios en cuatro niveles de bioseguridad en función de (i) la infectividad del patógeno, (ii) la severidad de la enfermedad causada, (iii) el grado de transmisibilidad, (iv) el origen del agente (exótico o no) y, (v) la naturaleza del trabajo llevado a cabo en el inmueble (2). Cada nivel de bioseguridad refleja el tipo de prácticas microbiológicas, el tipo de equipo y las medidas de seguridad tomadas en ese laboratorio en particular (18). En general, se procura lograr un ambiente de trabajo seguro para el personal y para las personas ajenas al laboratorio, incluyendo las que se encuentran fuera de las instalaciones.
De acuerdo al CDC, los cuatro niveles de bioseguridad son los siguientes (2) (Cuadro II).
• Nivel 1 (BSL-1): prácticas, equipo y medidas adecuadas para el nivel de enseñanza. El trabajo se realiza con cepas definidas y caracterizadas de microorganismos que no causen enfermedad en humanos adultos sanos. No se necesita el uso de equipo especial de protección, con el equipo básico es suficiente.
• Nivel 2 (BSL-2): prácticas, equipo y medidas adecuadas para laboratorios de análisis, diagnóstico o patología clínica donde se manejen microorganismos de riesgo moderado que están presentes en la comunidad y se encuentran asociados a enfermedades humanas de severidad variable.
• Nivel 3 (BSL-3): prácticas, equipo y medidas adecuadas para laboratorios de análisis/diagnóstico clínico no conocidos que potencialmente puedan transmitirse por aerosol o salpicaduras y, que puedan causar una infección potencialmente letal.
• Nivel 4 (BSL-4): prácticas, equipo y medidas adecuadas para laboratorios de análisis/diagnóstico clínico e investigación que involucren la manipulación de agentes exóticos peligrosos que representen un gran riesgo por causar enfermedades letales, que puedan transmitirse vía aerosol y, para los cuales no haya vacuna ni terapia conocida.
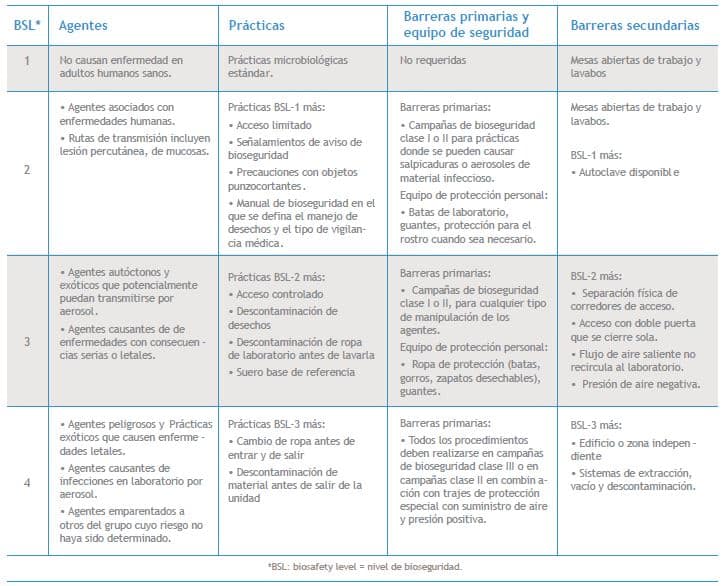
Cuadro 2. Medidas generales de bioseguridad correspondientes a cada nivel 3
De los cuatro niveles mencionados, en los últimos dos se manejan agentes patógenos considerados como potencialmente peligrosos por las posibilidades que existen del surgimiento de un subtipo pandémico o por haber dado origen a una epidemia no controlada (patógenos emergentes y reemergentes respectivamente) (19). Los laboratorios de bioseguridad nivel 3 y 4 son herramientas esenciales en la investigación por brindar la posibilidad de aislar, cultivar y preservar estos microorganismos en su estado activo.
En cada laboratorio debe existir una persona encargada de la valoración de riesgo para seleccionar de forma adecuada el nivel de contención en el que se debe trabajar (10). El proceso de valoración de riesgo involucra, de acuerdo a Barkley, cuatro pasos básicos:
(i) identificación de los factores de riesgo (peligros relacionados al agente, al protocolo y a la susceptibilidad a la enfermedad); (ii) evaluación de la posibilidad de una exposición (de personas que lleven a cabo el protocolo, de personas presentes en el laboratorio y de personas no asociadas al laboratorio); (iii) evaluación de las consecuencias potenciales de una exposición; (iv) evaluación de la capacidad de las medidas de seguridad para controlar el riesgo (10).
Además de los factores mencionados, de acuerdo al Ministerio de Salud de Canadá se debe tomar en cuenta el potencial para generar aerosoles, la cantidad, la concentración, la estabilidad ambiental del agente, el tipo de trabajo propuesto (in vitro, in vivo) y el uso de organismos recombinantes (por ejemplo: genes que codifican para factores de virulencia o toxinas, alteración del rango de hospedero, oncogenicidad, capacidad de revertir al tipo silvestre) (16).
La Organización Mundial de la Salud, mediante el Reglamento Sanitario Internacional (2005), estipula otras recomendaciones relacionadas a la bioseguridad en el laboratorio, las cuales tienen como objetivo “prevenir la propagación internacional de enfermedades, proteger contra esa propagación, controlarla y darle una respuesta de salud pública proporcionada y restringida a los riesgos para la salud pública”. Este reglamento debe ser cumplido por los Estados Miembros (México incluido), a los que se les insta a que movilicen los recursos necesarios para lograrlo (20).
IV. Implementación de las políticas en los laboratorios
Los cuatro niveles de bioseguridad implican medidas particulares para cubrir estas necesidades. Además de ello, existen normas básicas de bioseguridad que todo laboratorio debe seguir sin importar el tipo de patógeno que maneje. Como se puede ver, la bioseguridad es un tema que compete a todas las personas que realicen actividades dentro de un laboratorio. Estas medidas no sólo se aplican a laboratorios de investigación, los laboratorios de análisis y diagnóstico clínico, los de patología, los industriales y los de enseñanza en los diferentes niveles educativos deben mantener una reglamentación general de bioseguridad. El Occupational Safety and Health Administration (OSHA) de los Estados Unidos, en la regulación 1910-1030, establece claramente los siguientes lineamientos (15,21):
1. Diseño de un manual de bioseguridad para eliminar o minimizar la exposición laboral a patógenos, el cual debe estar a disposición de cada persona del laboratorio. Este manual debe ser revisado anualmente por elsupervisor o director del laboratorio para hacer los cambios pertinentes al sistema de bioseguridad.
2. Identificación de sitios, tareas y procedimientos en los que podría ocurrir una exposición ocupacional.
3. Control de prácticas laborales:
- Lavarse las manos al quitarse el equipo de protección personal y después del contacto con sangre u otro material potencialmente infeccioso (Figura 1 a).
- No doblar, quitar o tapar de nuevo jeringas. Esta medida es muy importante, ya que la mayoría de los accidentes laborales ocurren al tapar de nuevo la aguja de la jeringa recién utilizada.
- No ingerir alimentos ni bebidas, no fumar, no aplicarse cosméticos ni manipular lentes de contacto en áreas de trabajo.
- No guardar comida ni bebidas en refrigeradores, cuartos fríos, congeladores, gabinetes o anaqueles donde se encuentre material potencialmente infeccioso.
- No pipetear con la boca.
4. Equipo de protección personal
- Varía de acuerdo al tipo de laboratorio. Debe utilizarse de forma obligada si se va a trabajar con material potencialmente infeccioso. Incluye: guantes, batas, máscaras, lentes y cubrebocas, entre otros (Figura 1 b y c).
- Los guantes desechables no deben lavarse o descontaminarse para su reutilización.
- Utilizar guantes siempre que se entre en contacto con sangre o material biológico-infeccioso (Figura 1 c)
5. Limpieza: el área y equipo de trabajo debe mantenerse siempre limpio y descontaminado.
- La Environmental Protection Agency de los Estados Unidos provee una lista de los desinfectantes adecuados para evitar la contaminación por bacterias o virus en su página de Internet http://www.epa.gov/oppad001/chemregindex.htm (22).
Los ejemplos más comunes son etanol, hipoclorito de sodio, formaldehído, peróxido de hidrógeno y desinfectantes modernos de amplio espectro (18).
6. Manejo adecuado de desechos (vide infra).
7. Etiquetado de equipo y material: el símbolo de bioseguridad debe ser utilizado para identificar contenedores de desechos, refrigeradores y congeladores que contengan material potencialmente infeccioso (Figura 1 d).
8. Información y entrenamiento del personal: las personas que realicen cualquier actividad en un laboratorio deben estar informadas del nivel de bioseguridad al que pertenece, de los patógenos que maneja y del riesgo que corre al encontrarse allí.

Figura 1. (ver a la derecha) Elementos de seguridad dentro de un laboratorio. (a) El laboratorio debe incluir un sitio para lavarse las manos.También se muestra una regadera de ojos para limpiarlos si hay contacto con algún agente infeccioso. (b) Equipo de protección personal utilizado en un laboratorio de bioseguridad nivel 3: guantes, gorro y batas desechables. (c) El uso de guantes es indispensable para manipular muestras que potencialmente puedan estar infectadas. (d) Símbolo universal de bioseguridad.
Además, debe estar entrenada para responder ante cualquier contingencia.
En todos los casos, siempre se deben tomar en cuenta las llamadas “precauciones universales”, conjunto de precauciones diseñadas para prevenir la transmisión del VIH, virus de la hepatitis B (VHB) y otros patógenos de transmisión sanguínea. Las precauciones universales involucran el uso de barreras de protección (guantes, batas, máscaras, lentes) que permitan reducir la exposición de piel o mucosas del profesional de la salud a materiales potencialmente infectivos. Además, incluyen recomendaciones para prevenir lesiones causadas por agujas, escalpelos u otros objetos punzocortantes (23,24).
El principio general de las precauciones universales es manejar toda sangre y fluidos corporales humanos como si estuvieran infectados con VIH, VHB, virus de la hepatitis C (VHC) u otros patógenos de este tipo. En particular, estos lineamientos aplican a sangre y otros fluidos que visiblemente contengan sangre, semen o secreciones vaginales, además de líquido cefalorraquídeo, sinovial, pleural, peritoneal, pericardial y amniótico. Las precauciones universales, de acuerdo a los CDC, no se aplican en el manejo de heces, secreciones nasales, esputo, sudor, lágrimas, orina y vómito (a menos que contengan sangre).
En el caso de la saliva no se toman en cuenta estas precauciones a menos que esté visiblemente contaminada con sangre (23).
V. Acciones correctivas frente a los accidentes laborales
El manejo de una exposición o un accidente laboral que involucre material infeccioso depende del microorganismo en particular que potencialmente pueda causar la infección. Todos los accidentes y exposiciones potenciales deben ser reportados inmediatamente al personal calificado. Después del incidente, se deben aplicar los cuidados médicos necesarios para remover el material infeccioso y para la administración de primeros auxilios (8). En caso de una herida, ésta debe lavarse con agua y jabón sin dañar la piel, las membranas mucosas expuestas deben irrigarse copiosamente con agua o solución salina. Si la herida se causó por un piquete de aguja se debe dejar fluir la sangre primero sin introducirla la boca (25). Además, se debe dar acceso al personal de laboratorio a consultas médicas confidenciales, asesoría médica sobre el riesgo que corre y tratamiento profiláctico (8).
El riesgo estimado de infección por VIH por lesiones causadas por agujas o algún otro tipo de exposición es del 0.3% por contacto. Para este virus, el tratamiento profiláctico consta de diferentes tipos de antirretrovirales, los cuales pueden llegar a disminuir hasta en un 80% la posibilidad de que se establezca la infección(26). Para el VHB, la medida profiláctica más recomendada es el uso de la vacuna. En el caso del VHC, no hay profilaxis post-exposición disponible (27).
VI. Manejo de desechos biológico-infecciosos
Los residuos peligrosos biológico-infecciosos (RPBI), según la nomenclatura oficial en México, (Norma Oficial Mexicana NOM-087-ECOL-SSA1-2002 “Protección ambiental – Salud ambiental – Residuos peligrosos biológico- infecciosos – clasificación y especificaciones de manejo”) (28) deben ser manejados con gran cuidado para no generar focos de infección que puedan dañar al personal del laboratorio, a la población o al ambiente.
De acuerdo a la OMS, el 75-90% de los desechos de los laboratorios y hospitales son similares a los domésticos y, el 10-25% restante está compuesto por desechos peligrosos que requieren tratamiento especial.
El riesgo de este tipo de material está dado por la posibilidad de que contenga agentes infecciosos, punzocortantes, químicos o fármacos, sustancias genotóxicas o elementos radiactivos. Las fuentes más importantes de RPBI incluyen hospitales, clínicas, laboratorios, bancos de sangre, depósitos de cadáveres, clínicas dentales, farmacias, entre otros (27,29).
Durante la Conferencia de las Naciones Unidas sobre el Medio Ambiente y el Desarrollo se establecieron las recomendaciones para el manejo de desechos, las cuales se resumen en cuatro postulados: (i) prevenir y minimizar la producción de desechos, (ii) reutilizar o reciclar hasta donde sea posible, (iii) tratar los desechos con métodos seguros y que no dañen al ambiente, y (iv) disponer de ellos en sitios cuidadosamente diseñados y confinados (27).
La Organización Mundial de la Salud propone en su manual “Safe management of wastes from health-care activities”, (29) la clasificación de los residuos en nueve tipos, los cuales se describen en el Cuadro III. De ellos, los residuos infecciosos incluyen los cultivos de agentes infecciosos, los desechos de cirugía y autopsias en pacientes con alguna enfermedad infecciosa, los desechos de pacientes de salas de aislamiento, desechos que hayan estado en contacto con pacientes infectados durante la hemodiálisis, animales infectados de laboratorio y cualquier otro instrumento o material que haya estado en contacto con personas o animales infectados.
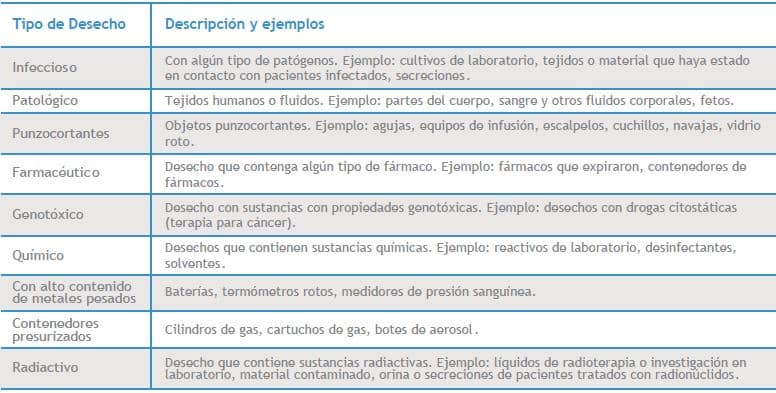
Cuadro 3. Clasificación, descripción y ejemplos de los desechos generados en el sector salud de acuerdo a la Organización Mundial de la Salud 25
Las posibilidades de supervivencia de un microorganismo patógeno en el ambiente están en función de su capacidad de resistir a condiciones ambientales como temperatura, humedad, radiación UV, disponibilidad de materiales orgánicos, presencia de predadores,etc. El VHB, por ejemplo, puede mantenerse viable por varias semanas en superficies secas, resiste la actividad de algunos antisépticos y del etanol al 70% y, sobrevive durante 1 semana en una gota de sangre dentro de una jeringa hipodérmica. En cambio, el VIH solamente resiste 15 minutos al ser expuesto a etanol al 70% y 3-7 días a temperatura ambiente. El peligro de los desechos infecciosos está en función de la carga microbiana que contengan que, en el caso de cultivos y de excreciones de pacientes infectados, puede ser alta. Aunado a ello, su mal manejo permite el contacto con vectores como ratas, ratones, moscas, cucarachas y otros insectos que se alimentan o se reproducen en desechos orgánicos, los cuales son acarreadores pasivos de agentes patógenos (27). Las infecciones causadas por la exposición a RPBI se indican en el Cuadro IV.
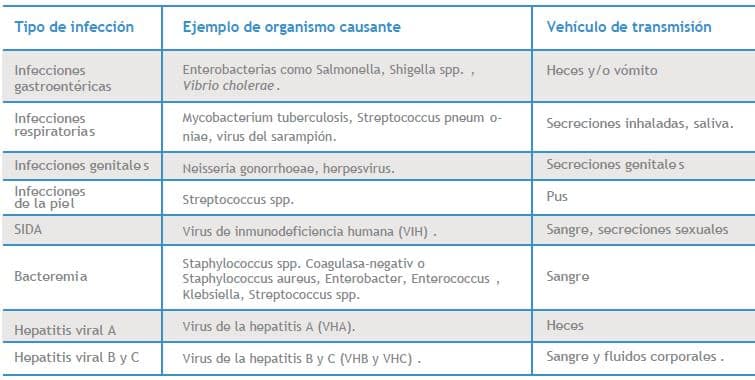
Cuadro 4. (ver a la derecha) Ejemplo de infecciones causadas por exposición a desechos biológico-infecciosos, organismos causantes y vehículos de transmisión 25
México es un gran productor de desechos biológico-infecciosos. La Organización Panamericana de la Salud (OPS) ha estimado que se generan 13,160 toneladas de RPBI en las 60,100 camas de hospital usadas al año en nuestro país (27). La NOM-087-ECOL-SSA1-2002, también establece los requisitos para el manejo de RPBI, los cuales define como “aquellos materiales generados durante los servicios de atención médica que contengan agentes biológico- infecciosos… y que puedan causar efectos nocivos a la salud y al ambiente.”
De acuerdo a esta norma, los RPBI se clasifican en: sangre, cultivos y cepas de agentes biológico-infecciosos, patológicos, residuos no anatómicos y objetos punzocortantes. Cada uno de ellos debe ser identificado, envasado, almacenado, recolectado, transportado y tratado de forma particular. El laboratorio de análisis y diagnóstico clínico debe envasar los residuos líquidos en recipientes herméticos rojos (sangre, residuos no anatómicos) o amarillos (patológicos) y los residuos sólidos en bolsas de polietileno rojas (cultivos y cepas de agentes infecciosos, residuos no anatómicos) o amarillas (patológicos) (Figura 2a). En caso de desechar objetos punzocortantes debe de hacerse en recipientes rígidos de polipropileno rojo (Figura 2 b) (28).

Figura 2. (a) Bolsas de polietileno rojas para desecho de cultivos y cepas de agentes infecciosos además de residuos no anatómicos. (b) Contenedores rígidos de polipropileno rojo para desechos punzocortantes. La aguja se desecha sin taparla de nuevo utilizando guantes.
Los contenedores utilizados son especiales para evitar rasgaduras o filtraciones, por lo que es importante comprar los que cumplan con las características mencionadas ya que, de no ser así, su uso es inadecuado.
Existen en el mercado bolsas rojas de material muy delgado semitransparente que se venden con esta finalidad, pero que no son de propileno y no son resistentes a las rasgaduras. Antes de comprar material de baja calidad hay que recordar los riesgos que se corren si el material biológico-infeccioso no es manipulado de forma adecuada y hay que tomar en cuenta que tampoco se cumple con la NOM-087- ECOL-SSA1-2002.
VII. Panorama de la bioseguridad en México
En México, la regulación de la bioseguridad está dada en la Ley General de Salud, que en su artículo 146 (Título octavo, capítulo II) establece que “los laboratorios que manejen agentes patógenos estarán sujetos a control por parte de las autoridades sanitarias competentes… en lo relativo a las precauciones higiénicas que deban observar, para evitar la propagación de las enfermedades transmisibles al hombre” (30). La Secretaría de Salud ejerce las atribuciones de regulación, control y fomento sanitarios a través de la Comisión Federal para la Protección contra Riesgos Sanitarios (COFEPRIS), a la cual compete “identificar y evaluar los riesgos para la salud humana que generen los sitios en donde se manejen residuos peligrosos”, es decir, establecimientos donde se manejen órganos, tejidos, células de seres humanos y sus componentes, sangre, medicamentos y otros insumos para la salud, sustancias tóxicas o peligrosas para la salud, químicos esenciales, precursores químicos, productos biotecnológicos, entre otros (Art. 17 bis LGS) (30, 31).
Para los laboratorios clínicos, en la Norma Oficial Mexicana NOM-166-SSA1-1997, “Para la organización y funcionamiento de los laboratorios clínicos”, (32) se dispone que cada uno debe contar con un responsable sanitario encargado de la aplicación de “las medidas de seguridad e higiene para la protección de la salud del personal expuesto por su ocupación”. Sin embargo, no especifica cuáles son las normas de bioseguridad correspondientes a seguir por los trabajadores.
En esta norma se recomienda consultar la bibliografía especializada en el área, que en este caso sería lo publicado por diferentes organismos como el CDC, la OSHA y la OMS. Además, también se recomienda consultar la Norma Oficial Mexicana NOM-003-SSA2-1993, “Para la disposición de sangre humana y sus componentes con fines terapéuticos” (33).
En lo referente al manejo del concepto de bioseguridad en laboratorios que manejan agentes patógenos, la reglamentación mexicana es similar a la de Estados Unidos. En el Reglamento de la Ley General de Salud en Materia de Investigación para la Salud, en el Título Cuarto, Capítulo I “De la investigación con microorganismos patógenos o material biológico que pueda contenerlos”, artículo 75, se menciona que las instituciones de salud donde se realice alguna investigación en la que se maneje algún patógeno deberán contar con las instalaciones y equipo de laboratorio adecuadas para la seguridad del personal, elaborar un manual de procedimientos, capacitar al personal, proveer de vigilancia médica, establecer un programa de supervisión y seguimiento de seguridad y disponer de bibliografía actualizada en el área (34).
A diferencia de lo manejado en los Estados Unidos, en el artículo 76 de este reglamento se clasifica a los laboratorios en tres tipos y no cuatro. A cada uno de ellos se le asigna el manejo de un grupo de riesgo (GR) de los cuatro establecidos en el artículo 79, los cuales coinciden con lo propuesto por los CDC y la OMS. Los tres tipos de laboratorios (artículo 80, 81, 82) son: Laboratorio básico de microbiología (GR1 y GR2), Laboratorio de seguridad microbiológica (GR3) y Laboratorio de máxima seguridad microbiológica (GR4). En cada uno de ellos debe existir un investigador responsable que definirá “el tipo de laboratorio en el que deberá realizar las investigaciones propuestas, así como los procedimientos respectivos, tomando en cuenta el grado de riesgo de infección que presenten los microorganismos a utilizar.” (Art. 78) (34).
Comentarios
La idea de bioseguridad surgió para proteger a las personas que, ya sea por trabajo o por estudio, lleguen a estar en contacto con algún patógeno o muestra potencialmente infecciosa. En nuestro idioma, esta palabra cuenta con distintas acepciones. Por una parte se le relaciona con las medidas que se toman durante la vigilancia epidemiológica para prevenir brotes de alguna enfermedad o situaciones peligrosas como el bioterrorismo.
Por otra parte, bioseguridad hace referencia a las medidas relacionadas con el trabajo seguro en el laboratorio. En inglés, la primera acepción se traduce como biosecurity y la segunda como biosafety. Varios son los libros, manuales y artículos que se han escrito sobre este tema y, sin embargo, las infecciones adquiridas en el laboratorio siguen sucediendo. Seguir los reglamentos mencionados (CDC, OMS, OSHA, SSA) podría minimizar o evitar la posibilidad de sufrir un accidente laboral.
Como responsables o miembros de un laboratorio, tenemos la obligación de conocer las medidas de bioseguridad relativas a nuestro trabajo. Para ello, debemos de ser capaces de identificar el grupo de riesgo al que pertenece el patógeno con el que estemos en contacto y, el nivel de bioseguridad al que corresponde el laboratorio. También debemos estar al tanto de las precauciones universales que se deben de tomar en cualquier tipo de instalación.
Nunca hay que olvidar que la bioseguridad es un concepto aplicable a cualquier área de las ciencias de la salud, no es exclusiva del área académica o de investigación.
En los laboratorios de análisis o diagnóstico clínico, diversos agentes patógenos son muestreados y aislados antes de siquiera ser manipulados para llevar a cabo una investigación. En la mayoría de los casos, los profesionales del laboratorio somos los primeros en enfrentarnos a ellos. La aplicación de las medidas de bioseguridad y el uso de técnicas y equipo adecuado permitirán prevenir accidentes laborales en el laboratorio. Como la OMS señala, ninguna campaña de bioseguridad ni algún otro tipo de equipo o procedimiento por sí solos garantizan la seguridad del trabajador, a menos que se opere bajo las normas de bioseguridad establecidas y el personal esté consciente del riesgo al que se enfrenta.
Con base en los textos consultados y en nuestra experiencia, sugerimos a los laboratorios clínicos hacer un manual de bioseguridad propio donde incluyan las reglas básicas de bioseguridad particulares a su área de trabajo, el nivel de riesgo de los microorganismos con los que se tiene contacto, el nivel de bioseguridad del laboratorio y la forma de manejo de desechos biológico-infecciosos. En el manual de bioseguridad se deben incluir los procedimientos administrativos a seguir en caso de modificaciones a las reglas de bioseguridad o de alguna infección laboral.
Además, en los protocolos de trabajo ya establecidos para cada proceso realizado en el laboratorio se tiene que incluir un anexo con las precauciones de bioseguridad que se deben tomar en ese procedimiento en particular, haciendo énfasis en las situaciones de riesgo que se pueden dar (ejemplo, generación de aerosoles).
En el manual se podría anexar el listado de grupos de riesgo y los patógenos que lo incluyen, así como las características de cada nivel de bioseguridad.
En el laboratorio debe haber un responsable o una comisión responsable de vigilar que se cumplan las normas de bioseguridad mediante la revisión rutinaria de los laboratorios. Las personas que integrenesta comisión deben tener la preparación adecuada en el área y deben tener a la mano textos nacionales e internacionales del área, como el manual de bioseguridad del CDC o de la OMS y las normas mexicanas.
Estas medidas permitirán verificar y mejorar la organización y el funcionamiento de la bioseguridad en el laboratorio clínico.
Conclusiones
El trabajo en el laboratorio clínico implica riesgos para el personal que está en contacto con material biológico-infeccioso. Los laboratorios clínicos, por ende, son sitios donde el concepto de bioseguridad debe formar parte de la vida diaria de cada persona.
Las medidas de bioseguridad deben estar claramente definidas en un manual y deben ser conocidas y estar al alcance de la mano de todos. Organismos internacionales como el CDC, la OMS y la OSHA juntos con la Secretaría de Salud en México establecen, dentro de sus publicaciones o reglamentos, cuáles son los lineamientos a seguir en el trabajo del laboratorio clínico, cuál es el grupo de riesgo al que cada patógeno pertenece, las características de cada nivel de bioseguridad, las medidas en caso de accidentes y el manejo de desechos biológico-infecciosos.
En el presente artículo presentamos de forma general esta información para que esté al alcance de laboratorios clínicos del país y que la puedan utilizar como base para generar sus propios reglamentos de bioseguridad.
Agradecimientos
Agradecemos la valiosa colaboración de la Dra. Ana Flisser Steinbruch, Presidenta de la Sociedad Mexicana de Parasitología, A.C., por revisar y comentar el presente texto.
Referencias Bibliográficas
1. Madigan MT, Martinko JM, Parker JB. Biología de los microorganismos. 8a ed. Madrid: Prentice all Iberia; 1999: p. 15-29.
2. U.S. Department of Health and Human Services, Centers for Disease Control and Prevention, National Institutes of Health. Biosafety in microbiological and biomedical laboratories. 5a ed. Washington: Oficina de Imprenta del Gobierno de los Estados Unidos; 2007. p. 1-113.
3. University of California, Irving. UCI Biosafety handbook. Rev. 2005. [Consultada en agosto 2007] Disponible en: http://www.ehs.uci.edu/programs/biosafetiyo S/bafety_handBook/index.html
4. Do AN, Ciesielski CA, Metler RP, Hammett TA, Li J, Fleming PL. Occupational acquired human immunodeficiency virus (HIV) infection: national case surveillance data during 20 years of the HIV epidemic in the United States. Infect Control Hosp Epidemiol. 2003; 24: 86-96.
5. Petrosillo N, Puro V, De Carli G, Ippolito G. Risks faced by laboratory workers in the AIDS era. J Biol Regul Homeost Agents. 2001; 15: 243-8.
6. Pike RM. Laboratory-associated infections: summary and analysis of 3921 cases. Health Lab Sci. 1976; 13(2): 105-14.
7. Herman P. Laboratory-acquired Infections: Introduction. Belgian biosafety server. 2007. [Consultada en septiembre 2007]. Disponible en: http://www.biosecurite.be/CU/LAI/Intro_LAI.html
8. Sewell DL. Laboratory-associated infections and biosafety. Clin Micro Rev. 1995; 8: 389-405.
9. Health and Safety Office, University of North Carolina at Chapel Hill. Biological safety manual. 2000. [Consultada en septiembre 2007] Disponible en: http://ehs.unc.edu/manuals/bsm/
10. Barkley WE. Risk assessment and containment. Howard Hughes Medical Institute. 2004. [Consultada en agosto 2007] Disponible en: http://www.webconferences.com/nihoba /ppt/Risk%20Assessment% 2009-21-04_Barkley.pdf.
11. Bavoil PM. Federal indifference to laboratory-acquired infections. Appl Biosafety. 2005; 3: 105-7.
12. Lewis FM, Chernak E, Goldman E, Li Y, Karem K, Damon IK, et al. Ocular vaccinia infection in laboratory worker, Philadelphia 2004. Emerg Infect Dis. 2006; 12: 134-7.
13. Wagenvoort JH, De Brauwer EI, Gronenschild JM, Toenbreker HM, Bonnemayers GP, Bilkert- Mooiman MA. Laboratory-acquired meticillin- resistant Staphylococcus aureus (MRSA) in two microbiology laboratory technicians. Eur J Clin Microbiol Infect Dis. 2006; 25: 470-2.
14. Centers for Disease Control and Prevention. Salmonella serotype enteritidis infections among workers producing poultry vaccine, Maine. November – December 2006. Morbidity and mortality weekly report, Centers for Disease Control and Prevention. 2007; 56; 877-9.
15. Minister of Health Population y Public Health Branch Centre for Emergency Preparedness and Response from Canada. The laboratory biosafety guidelines. 3a ed. 2004. [Consultada en agosto 2007] Disponible en: http://www.phacaspc.gc.ca/ols-bsl/lbg-ldmbl/index.html
16. Organización Mundial de la Salud. Laboratory biosafety manual. 3a ed. Génova: Organización Mundial de la Salud; 2004.
17. Liberman DF, Harding LA. Biosafety: the research/diagnostic laboratory perspective. En: Liberman DF, editor. Biohazards management handbook. 2a. ed. Estados Unidos:Marcel Dekker; 1995. p. 151-71.
18. Flanders Interuniversity Institute for Biotechnology. Biosafety in the laboratory. VIB publication. Bélgica: Flanders Interuniversity Institute for Biotechnology; 2004. p. 9-13.
19. Mesa G, Rodríguez I, Teja J. Las enfermedades emergentes y reemergentes: un problema de salud en las Américas. Rev Panam Salud Publ. 2004; 15; 285-7.
20. Organización Mundial de la Salud. Revisión del Reglamento Sanitario Internacional. 2005. [Consultada en agosto 2007]. Disponible en: http://www.who.int/gb/ebwha/pdf_files/WHA58 /WHA58_3-sp.pdf
21. Occupational Safety and Health Administration. Bloodborne pathogens.- 1910.1030. [Consultada en septiembre 2007] Disponible en: http://www.osha.gov/pls/oshaweb /owadisp.show_document?p_table= STANDARDS&p_id=10051
22. US Environmental Protection Agency. Selected EPA-registered disinfectants. [Consultada en octubre 2007] Disponible en: http://www. epa.gov/oppad001/chemregindex.htm
23. Centers for Disease Control and Prevention. Universal precautions for prevention of transmission of HIV and other bloodborne infections. 1996. [Consultada en agosto2007] Disponible en: http://www.cdc. gov/ncidod/dhqp/bp_universal_precautions.html
24. Occupational Health Service, Queen Mary University of London. Universal precautions. [Consultada en agosto 2007] Disponible en: http://www.ohs.qmul.ac.uk /Universal%20Precautions.htm
25. UK Health Departments. Guidance for Clinical Health Care Workers: Protection against infection with blood-borne viruses. [Consultada en agosto 2007] Disponible en: http://www.dh.gov.uk/prod_consum_dh/groups/dh_digitalassets/@ dh/@en/documents/digitalasset/dh_4014474.pdf
26. Tashima K, Weiss M. Prevention of HIV transmission after health care worker occupational exposure. Med Health R I. 2003; 86: 172-4.
27. Pruess A, Giroult E, Rushbrook P. Safe management of wastes from health-care activities. Ginebra, Suiza: Organización Mundial de la Salud; 1999.
28. Norma Oficial Mexicana. NOM-087-ECOL-SSA1-2002. Protección ambiental – Salud ambiental – residuos peligrosos biológico infecciosos – Clasificación y especificaciones de manejo. Diario Oficial de la Federación, 17 de febrero de 2003.
29. Organización Mundial de la Salud. Wastes from healthcare activities. Fact sheet No. 253. October 2000. [Consultada en agosto 2007] Disponible en: http://www.who.int/mediacentre /factsheets/fs253/ en/
30. Ley General de Salud. Diario Oficial de la Federación, 7 de febrero de 1984.
31. Comisión Federal para la Protección contra Riesgos Sanitarios. Marco jurídico. [Consultada en agosto 2007] Disponible en: http:// www.cofepris.gob.mx/mj/mj.htm
32. Norma Oficial Mexicana. NOM-166-SSA1-1997. Para la organización y funcionamiento de los laboratorios clínicos. Diario Oficial de la Federación, 4 de diciembre de 1998.
33. Norma Oficial Mexicana. NOM-003-SSA2-1993. Para la disposición de sangre humana y sus componentes con fines terapéuticos. Diario Oficial de la Federación, 8 de diciembre de 1993.
34. Reglamento de la Ley General de Salud en Materia de Investigación para la Salud. Diario Oficial de la Federación, 6 de enero de 1987.






