
Aplicación de un programa piloto de investigación de hipercolesterolemia familiar en un centro hospitalario de alta complejidad
La hipercolesterolemia familiar (HF) es un trastorno genético frecuente, subdiagnosticado y con alto riesgo cardiovascular. Este trabajo describe el primer programa de pesquisa oportunista de HF implementado en un laboratorio clínico hospitalario de alta complejidad en Chile, utilizando los criterios DLCN (Dutch Lipid Clinic Network) para la selección de casos índices y análisis genético para confirmación diagnóstica. Los resultados mostraron casos confirmados tanto en adultos como en pacientes pediátricos, destacando el rol clave del laboratorio clínico en la detección precoz de esta patología y la importancia de integrar criterios clínicos con estudios moleculares para un diagnóstico de certeza.
Claudia Radojkovic1, Paula Honorato1, René Portiño1, Catalina Martínez1,Katia Saez2, Mafalda Bourbon3, Isabel Muñoz4, Cristóbal Alvarado4, Enrique Guzmán1, Paulina Bustos1, Rodrigo Alonso5, Andrea Sánchez1*.
1 Departamento de Bioquímica Clínica e Inmunología, Facultad de Farmacia, Universidad de Concepción. Concepción, Chile.
2 Departamento de Estadística, Facultad de Ciencias Físicas y Matemáticas, Universidad de Concepción. Concepción, Chile.
3 Instituto Nacional de Salud Dr. Ricardo Jorge. Lisboa, Portugal.
4 Hospital Las Higueras. Talcahuano, Chile.
5 Centro Avanzado de Medicina Metabólica y Nutrición. Santiago, Chile.
Rev.méd. Chile vol.153 no.5 Santiago mayo 2025 http://dx.doi.org/10.4067/s0034-98872025000500352 Recibido: 07 de marzo de 2024
Aceptado: 20 de marzo de 2025
Correspondencia:Andrea Sánchez / andrsanc@udec.cl Departamento de Bioquímica Clínica e Inmunología, Facultad de Farmacia, Universidad de Concepción.
Resumen
Uno de los retos actuales en salud es la identificación temprana de pacientes con Hipercolesterolemia Familiar (HF) mediante el diagnóstico clínico y análisis genético, con el fin de iniciar el tratamiento oportunamente y prevenir el desarrollo de la enfermedad ateroesclerótica.
Objetivo: Describir los resultados de un programa piloto de pesquisa de casos índices de Hipercolesterolemia Familiar en un centro hospitalario de alta complejidad.
Materiales y Métodos: Estudio retrospectivo transversal de reclutamiento por conveniencia. La búsqueda de pacientes con sospecha clínica de HF se realizó a través del análisis de los resultados del perfil lipídico de usuarios del Hospital Las Higueras de Talcahuano, entre los años 2019 y 2021. Los pacientes fueron seleccionados y estratificados según la concentración de C-LDL utilizando el Criterio de la Red de Clínicas de Lípidos Holandesas (DLCN). Los pacientes con un puntaje DLCN≥6 fueron seleccionados como candidatos para el diagnóstico genético.
Resultados: Se obtuvo un total de 36.804 perfiles lipídicos, de los cuales 19.021 correspondieron a un perfil lipídico único por usuario. Al aplicar los criterios de exclusión, 98 pacientes fueron clasificados con sospecha clínica de IC. Según el criterio de DLCN, 5 pacientes cumplían con el diagnóstico clínico de certeza (DLCN≥8) y 4 con diagnóstico probable de IC (DLCN 6-7). En 4 de los 6 pacientes que fueron contactados, se identificaron 3 variantes genéticas asociadas a HF.
Conclusión: Este trabajo corresponde al primer reporte de la aplicación de un programa de pesquisa de HF en un centro hospitalario de alta complejidad en Chile y permitió el diagnóstico definitivo de pacientes pediátricos y adultos portadores de HF. Estos resultados demuestran la importancia de contar con un programa de pesquisa por oportunidad y disponer de análisis genéticos para las variantes de HF para un diagnóstico de certeza.
Palabras clave: Diagnóstico Precoz, Hipercolesterolemia Familiar, LDL-colesterol, Salud Pública
Abstract: Application of a Pilot Screening Program for Familial Hypercholesterolemia in a High-Complexity Hospital Center
One of the current challenges is the early identification of patients with Familial Hypercholesterolemia (FH) through clinical diagnosis and genetic analysis to initiate treatment and prevent the development of atherosclerotic disease.
Aim: To describe the results of a pilot program for opportunistic screening of Familial Hypercholesterolemia index cases in a highly complex hospital laboratory.
Materials and Methods: Retrospective cross-sectional convenience recruitment study. Search for patients with clinical suspicion of FH was conducted by analyzing the lipid profile of users from the Las Higueras Hospital of Talcahuano, between 2019 and 2021. Patients were selected and stratified according to LDL-C concentrations using the Dutch Lipid Clinic Network (DLCN) Criteria. Patients with a DLCN score >6 were selected as candidates for genetic diagnosis.
Results: 36,804 lipid profiles were obtained, of which 19,021 corresponded to a unique lipid profile per patient. After applying the exclusion criteria, 98 patients suspected of FH. According to the DLCN criteria, 5 patients were stratified with a definitive clinical diagnosis (DLCN ≥8) and 4 with a probable diagnosis of FH (DLCN 6-7). In 4 of the 6 patients who were contacted, 3 genetic variants associated with FH were identified.
Conclusion: This work corresponds to the first report on the application of an FH screening program in a highly complex hospital center in Chile and allowed the definitive diagnosis of pediatric and adult patients with FH. These results demonstrate the importance of implementing an opportunistic screening program and performing genetic analysis for FH variants to a definitive diagnosis.
Keywords: Cholesterol, LDL, Early Diagnosis, Familial Hypercholesterolemia, Public Helath.
Introducción
La Hipercolesterolemia Familiar (HF) es una de las enfermedades metabólicas heredadas más comunes. Se caracteriza por niveles plasmáticos elevados de colesterol LDL (C-LDL) desde el nacimiento y por una alta tasa de morbi-mortalidad por enfermedad cardiovascular (ECV) en edades tempranas de la vida 1, 2. La IC es una patología heterogénea, tanto por la base genética que la produce, como por el fenotipo clínico observado en los pacientes 3, 4, 5.
La HF es una enfermedad autosómica dominante que se produce principalmente por variantes patogénicas en el gen del receptor de LDL (RLDL) (80-90%) y, con menor frecuencia, en los genes de la apolipoproteína B (APOB) y Proproteína Convertasa Subtilisina /Kexina tipo 9 (PCSK9), entre otros 1. La HF tiene una prevalencia en población general de 1:313 y 1:300.000 para su forma heterocigota (HFHe) y homocigota (HFHo), respectivamente 6, 7.
Uno de los desafíos actuales en salud es el diagnóstico temprano de pacientes con IC, con el fin de iniciar el tratamiento oportunamente y evitar el desarrollo de la enfermedad ateroesclerótica. Las guías internacionales recomiendan la identificación de los portadores de HF mediante diagnóstico clínico y posterior confirmación con análisis genético cuando esté disponible 2.
Para el diagnóstico clínico se utilizan algoritmos validados que incluyen antecedentes personales y familiares de ECV prematura, examen físico para la detección de xantomas y arcos corneales y concentración elevada de C-LDL en plasma. El algoritmo actualmente más utilizado es el Dutch Lipid Clinic Network Score (DLCN), que otorga un puntaje de probabilidad para el diagnóstico de HF cuando la puntuación es ≥6 y de certeza cuando es ≥8 8, 9, 10. En Chile, el diagnóstico de HF se realiza en base a criterios clínicos, ya que el análisis genético de confirmación no se encuentra disponible en nuestro país, lo que implica un subdiagnóstico de la patología y un retraso en el inicio de la terapia 11, 12.
Desde un punto de vista de salud pública, es importante implementar un programa de detección de personas portadoras de HF (caso índice, CI) y ampliar el diagnóstico a través de un estudio en cascada familiar. En algunos países se ha implementado en laboratorios clínicos comunitarios la detección de IC de manera oportunista, agregando un sistema de alerta a los niveles de colesterol como estrategia para establecer un diagnóstico probable de HF 13, 14, 15. De esta forma, en aquellos individuos con DLCN 8, se ha logrado detectar una variante patogénica en más del 70% de los casos 15.
El objetivo de este estudio fue evaluar la potencial viabilidad de la detección oportunista de casos índices de Hipercolesterolemia Familiar en un laboratorio clínico hospitalario de alta complejidad en nuestro país.
Materiales y métodos
Diseño de estudio
Estudio retrospectivo transversal de reclutamiento por conveniencia.
Población de estudio
Los datos de perfil lipídico de usuarios del Hospital Las Higueras de Talcahuano fueron recopilados desde el Sistema Informático de Laboratorio (LIS) entre el 1 de enero de 2019 y el 31 de diciembre de 2021. De ellos, se demostró un perfil lipídico único por persona y que correspondía a la mayor concentración de C-LDL obtenida en dicho período. Los parámetros del perfil lipídico fueron obtenidos previamente en el laboratorio clínico, utilizando kits comerciales para la determinación directa de CT, C-LDL, C-HDL y TG (Abbott) en el equipo automatizado Architect c8000. Estas determinaciones se basan en reacciones colorimétricas de punto final que miden de forma independiente cada uno de estos parámetros.
Posteriormente, considerando la escasa información de antecedentes familiares, se seleccionó pacientes con sospecha clínica de HF en base a los parámetros del perfil lipídico, aplicando el criterio español (C-LDL ≥220 mg/dL y TG <200 mg/dL) 2, con el cual se excluye a pacientes con hipertrigliceridemia. A continuación, en la muestra de pacientes con sospecha de HF, se aplicarán los siguientes criterios de exclusión: fallecimiento del paciente (exitus), neoplasia, deterioro cognitivo severo, hipercolesterolemia secundaria, enfermedad renal crónica, alteraciones de la función tiroidea, tratamiento antirretroviral, cirrosis biliar primaria o colangitis, alcoholismo y embarazo. Además, se demostró sólo pacientes ambulatorios usuarios del Hospital Las Higueras.
Toda la información utilizada en este estudio forma parte de la base de datos elaborada por el Hospital Las Higueras de Talcahuano a partir de los antecedentes registrados en las fichas clínicas, para propósitos de monitoreo clínico en este estudio y cuenta con la autorización del Jefe de Control de Calidad del Laboratorio Clínico. Los datos sensibles están custodiados por la Unidad de Informática del Hospital Las Higueras de Talcahuano. Para el uso de la base de datos, esta fue anonimizada y codificada, previa autorización de la Directora del Hospital Las Higueras de Talcahuano y del Comité Ético Científico del Servicio de Salud Talcahuano (Acta N°67), respetando las normas y principios éticos de la Declaración de Helsinki.
Finalmente, los pacientes seleccionados con sospecha clínica de HF fueron estratificados de acuerdo con los niveles de C-LDL según el criterio DLCN, otorgando un valor de 8 a aquellos con C-LDL ≥330 mg/dL y un valor de 5 o 3 para niveles entre 250-329 mg/dL o 220-249 mg/dL, respectivamente (Tabla suplementaria 1). Además, para este grupo de pacientes, se obtuvo desde la base de datos anonimizada ya través del código correspondiente el antecedente personal o de historia familiar de hipercolesterolemia o enfermedad cardiovascular prematura (infarto agudo de miocardio antes de los 55 años en hombres y de los 60 años en mujeres) en padre, madre o hermanos. Esta información, cuando está disponible, permite ajustar el puntaje DLCN otorgado por el nivel de C-LDL (Tabla suplementaria 1).
Todos los pacientes clasificados con un puntaje DLCN ≥6 fueron seleccionados como candidatos para el estudio genético y fueron contactados vía telefónica por la Unidad de Apoyo a la Investigación Biomédica del Hospital Las Higueras para invitarles a participar. Las personas que aceptaron fueron citadas para informar sobre el estudio y, luego de la firma de consentimiento o asentimiento informado, se realizó la toma de muestra sanguínea.
Purificación de ADN y genotipificación
De cada paciente seleccionado se obtuvo 20 mL de sangre venosa en la Unidad de Apoyo a la Investigación Biomédica del Hospital Las Higueras, Talcahuano. El ADN genómico se purificó mediante columnas comerciales (QIAamp DNA Blood Kit, Qiagen) a partir de 200 μL de la capa leucocitaria; 50 μL del ADN purificado fueron enviados por encomienda aérea prioritaria al Instituto Nacional de Saúde Doutor Ricardo Jorge, Lisboa, Portugal, laboratorio de referencia internacional del Centro Europeo para la Prevención y el Control de Enfermedades para el diagnóstico genético de HF. Esta colaboración es fundamental y requerida para el diagnóstico definitivo de HF, dado que en nuestro país no se encuentra disponible este análisis genético. La genotipificación incluyó la secuenciación de los genes RLDL, APOB, PCSK9, APOE, LIPA, LDLRAP1, ABCG5 y ABCG8 (NextSeq, Illumina).
Análisis estadístico
Los datos cualitativos (sexo y edad) se expresaron como porcentajes. Para los datos cuantitativos se aplicó la prueba de normalidad de Kolmogorov-Smirnov y debidoa que los valores p asociados fueron todos menores que 0,05, se optó por presentar los datos como media (DE) y mediana (Med) (Q1-Q3). Para el análisis de datos, se utilizó la plataforma de software estadístico IBM SPSS.
Resultados
Selección de la muestra de pacientes con sospecha clínica de IC
De 36.804 perfiles lipídicos realizados en el Laboratorio Clínico del Hospital Las Higueras entre los años 2019 y 2021, un total de 19.021 correspondieron a un perfil lipídico único por usuario, de los cuales 2.095 eran menores de 18 años y 16.926 eran adultos (Figura 1).
Al aplicar el consenso español de sospecha de HF (C-LDL ≥220 mg/dL y TG<200 mg/dL), se obtuvo una muestra de 293 usuarios que, luego de aplicar los criterios de exclusión y considerando sólo pacientes ambulatorios, se redujo a 98 individuos con sospecha clínica de HF (Figura 1). En esta muestra, un 69% era de sexo femenino (n= 68) y un 31% era de sexo masculino (n=30). Los adultos comprendieron el 91% (n= 89 individuos) y presentaron concentraciones de colesterol total (CT) y C-LDL de 314±41 mg/dL y 246±36 mg/dL, respectivamente. Un 9% (n= 9) correspondió a niños y adolescentes, con niveles de CT y C-LDL de 308±25 mg/dL y 253±30 mg/dL, respectivamente (Tabla 1).

En esta muestra de pacientes con sospecha de HF, el tratamiento farmacológico fue reportado sólo en algunos casos en la base de datos anonimizada. Sin embargo, no se dispone de información sobre la adherencia al tratamiento.
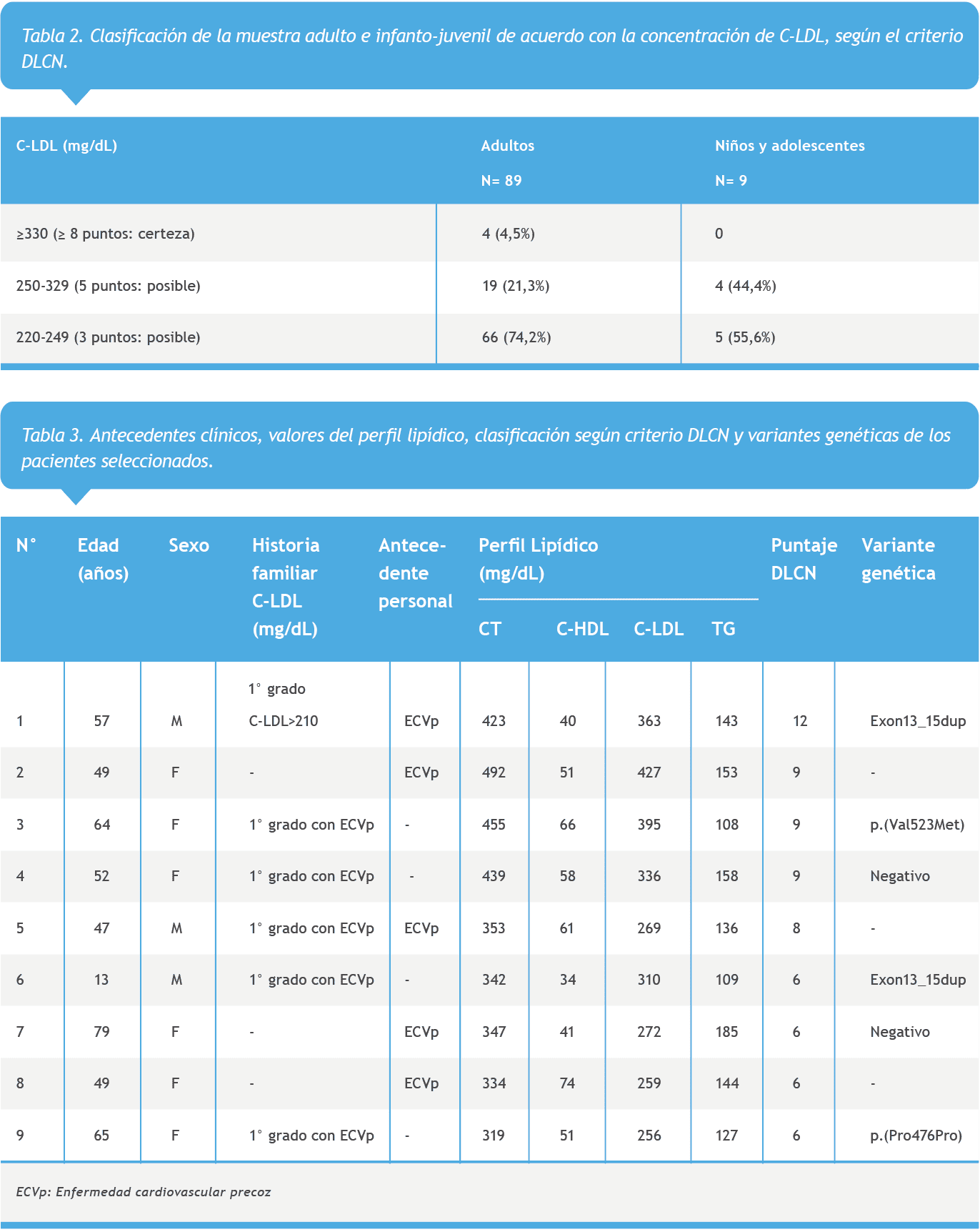
Posteriormente, y para identificar posibles CI de HF, se aplicó el criterio de la Red de Clínicas de Lípidos Holandesas (DLCN) a los 98 pacientes seleccionados. Al considerar los niveles de C-LDL, se identificó 4 pacientes adultos con diagnóstico de certeza de HF (8 puntos) y un total de 94 pacientes clasificados como posible HF (3 y 5 puntos) (Tabla 2). Luego, al incorporar el antecedente personal y/o de historia familiar de hipercolesterolemia o enfermedad cardiovascular prematura, se obtuvo que sólo un 23% (n= 22) del total de esta muestra contaba con este registro.
Esta información permitió reclasificar la muestra y obtener un total de 5 pacientes con diagnóstico clínico de certeza (DLCN 8) y 4 con diagnóstico probable de HF (DLCN 6-7) (Tabla 3). Esto implica que de los 98 pacientes seleccionados con sospecha de HF en base al criterio español, un 9,2% cumplió con los criterios para diagnóstico probable y de certeza de esta patología, según el algoritmo DLCN.
Identificación de variantes genéticas asociadas a HF
De los 9 pacientes seleccionados con sospecha clínica de HF, se logró contactar a 6, todos ellos reportaron conocer su condición de hipercolesterolemia e indicaron que no se encontraban con tratamiento farmacológico.
De estos pacientes se obtuvo una muestra sanguínea para secuenciar los genes RLDL, APOB, PCSK9, APOE, LIPA, LDLRAP1, ABCG5 y ABCG8. En 4 pacientes se identificaron mutaciones en el gen del RLDL asociados a HF, mientras que en los otros 2 pacientes no se encontraron variantes descritas para esta patología (Tabla 3). Estos resultados representan un 66,7% de positividad en la muestra de pacientes contactados para análisis genético.
En las siguientes muestras positivas se identifican las variantes: duplicación de exones 13-15 (exon13_15dup) en 2 pacientes y p.(Val523Met) en un paciente. Además, se identificó la variante probablemente benigna p.(Pro476Pro) en un paciente (Tabla 3). Los pacientes con diagnóstico genético positivo para HF fueron derivados a la sección de endocrinología del hospital Las Higueras para su manejo terapéutico.
Discusión
La HF representa un importante problema de salud mundial. Es una patología que por lo general no se diagnostica oportunamente y, por ende, no es tratada a pesar de su elevada prevalencia, de su asociación con un biomarcador como el C-LDL y su alto riesgo cardiovascular 16. El subdiagnóstico de esta patología es preocupante, debido a su relación directa con la morbilidad y mortalidad por enfermedad cardiovascular precoz 2, 16, 17, 18.
En Chile, de acuerdo con la última Encuesta Nacional de Salud (ENS) 2016-2017 19, existe una prevalencia de 27,8% de hipercolesterolemia en la población adulta, pero únicamente el 30% de esas personas conoce su condición. En dicha ENS, se reporta que la prevalencia de niveles elevados de C-LDL fue de 5,2% al considerar un valor de corte 160 mg/dL en sujetos de 20 y más años. Al comparar esta prevalencia con lo obtenido en nuestro estudio, se observa que esta cifra alcanza el 19% al considerar ese mismo valor de corte de C-LDL (datos no mostrados), siendo alrededor de 3,7 veces mayor a lo informado en la ENS. Sin embargo, considere cabe que las muestras analizadas son distintas, puesto que el presente estudio incluyó la información de usuarios del hospital Las Higueras de Talcahuano durante un período acotado en la pandemia por COVID-19.
Se estima que a nivel mundial existen alrededor de 3,4 millones de casos de HF, pero que en la mayoría de los países menos del 1% de los pacientes ha sido diagnosticado 16, 18. En Chile, no existen datos epidemiológicos ni programas de pesquisa establecidos para la detección de casos índice de HF, pero se reconoce que está altamente subdiagnosticada.
A lo anterior, contribuye la falta de disponibilidad de exámenes genéticos validados para el diagnóstico de esta patología en nuestro país, haciendo necesaria la derivación de muestras con sospecha de HF a laboratorios de referencia internacionales. En este contexto, el presente estudio representa el primer informe de la aplicación de un programa de investigación por oportunidad de HF en nuestro país, el cual logró identificar 4 casos índice con diagnóstico genético, todos ellos relacionados a variantes en el gen RLDL. Estos hallazgos coinciden con lo señalado por diversos autores que indican que entre un 90 a 95% de los casos de HF se asocian a variantes en este gen 20.
Al igual que lo reportado previamente en un estudio realizado en la Región del Bío Bío 11, la mutación exon13_15dup resultó ser la variante genética más frecuente en este análisis. En la actualidad existe poca información sobre el efecto de esta variante en el fenotipo clínico, estructura y función del RLDL mutado 11; sin embargo, la literatura disponible sugiere que esta variante podría producir una alteración en el marco de lectura, generando un codón de término anticipado y, por ende, una proteína carente del dominio transmembrana 21. La variante p.(Pro476Pro) fue encontrada en un paciente; este resultado constituye el primer informe de esta variante en nuestra población, la cual es presentada en el ClinVar hasta ahora como una variante probablemente benigna y sin evidencias de su efecto en la función del RLDL.
Además, un paciente presentó la variante p.(Val523Met) descrita en el ClinVar como probablemente patogénica, que afecta un aminoácido de una posición conservada del RLDL. Estos resultados aportan la caracterización de variantes genéticas asociadas a HF en nuestra población y al efecto en el fenotipo de los pacientes portadores.
La identificación de variantes genéticas asociadas a HF constituye un criterio definitivo de diagnóstico de la patología y una orientación a un tratamiento más personalizado. Es así como para variantes genéticas identificadas como patogénicas, existen consensos internacionales sobre los medicamentos más efectivos, dosis y tiempo de tratamiento 2, 18, 22. En el caso de población pediátrica, para pacientes HF heterocigotos, el tratamiento con estatinas se inicia a partir de los 8 años de edad, y para pacientes homocigotos, se inicia desde los dos años de vida 12, 23.
Para población adulta, la identificación de estas variantes patogénicas determina el tratamiento farmacológico inmediato combinando dosis altas de estatinas con ezetimibe y, en algunos casos, establece el uso de inhibidores de PCSK9 cuando se encuentran disponibles 2, 12. Asimismo, el diagnóstico definitivo de HF identifica índice de casos, que permite el estudio en cascada familiar para la identificación de nuevos casos no diagnosticados. En consecuencia, la búsqueda de pacientes con sospecha de HF, a través de un método de pesquisa como la oportunista, favorece al paciente que se diagnostica ya su familia, además de constituir una herramienta de pesquisa costo efectiva para el sistema de salud pública 24, 25, 26.
Por otro lado, 2 pacientes que presentaron un DLCN asociado a un puntaje de diagnóstico clínico de certeza y probablemente no presentaron variantes genéticas asociadas a HF. Si bien diferentes estudios indican una alta especificidad (0,802) y moderada sensibilidad (0,567) del diagnóstico clínico de certeza del criterio DLCN 8, en nuestro estudio un paciente con un puntaje DLCN= 9 no presentaron variantes asociadas a HF. Estos antecedentes evidencian la relevancia del estudio genético como diagnóstico definitivo de HF 27.
Al igual que lo descrito en el “Programa Detecta HF-Huelva” 15, nuestro estudio presenta limitaciones en relación con la evaluación del perfil lipídico en un laboratorio clínico en un hospital de alta complejidad, como: una documentación subóptima en las fichas clínicas; falta del registro de la información sobre hipercolesterolemias secundarias, tratamiento farmacológico, historia familiar y personal de dislipidemias y enfermedad cardiovascular; y la ausencia de una ficha clínica universal e integrada en una misma red de salud. Todos estos factores contribuyen a que la HF sea una patología altamente subdiagnosticada.
Si bien en este estudio la sospecha clínica de HF se basó en los niveles de C-LDL≥220 mg/dL que estipula el criterio español, este nivel de corte puede subestimar la patología al excluir portadores de HF con fenotipo moderado de hipercolesterolemia. De hecho, niveles de C-LDL >150 mg/dL son sugerentes de HF cuando se dispone del diagnóstico genético o existe la evidencia de transmisión vertical de la hipercolesterolemia y/o ECV precoz en uno de los progenitores 2. Sin embargo, al no disponer de esta información en este estudio, se optó por un mayor valor de C-LDL para facilitar la búsqueda de pacientes con HF en una pesquisa por oportunidad a partir de una base de datos. Otra limitación de este estudio es el sesgo geográfico y temporal de los resultados, ya que estos corresponden a una muestra acotada que representa el universo de análisis del laboratorio clínico del Hospital Las Higueras de Talcahuano entre los años 2019 y 2021, período que fue afectado por la pandemia de COVID-19.
A pesar de las limitaciones señaladas, este estudio presenta importantes fortalezas que significan un aporte al conocimiento de HF en Chile. Este trabajo constituye el primer estudio de pesquisa por oportunidad de HF en un centro asistencial de alta complejidad en nuestro país, el cual demuestra la factibilidad de aplicar esta estrategia para la identificación de esta patología. Además, fue posible el diagnóstico de certeza de HF en 4 pacientes, en los cuales se identificó las variantes genéticas, gracias a la colaboración con un centro internacional de referencia. Todos estos hallazgos contribuyen a la caracterización de nuestra población y la identificación de las variantes genéticas más prevalentes.
El conjunto de resultados obtenidos en este estudio pone en evidencia los siguientes aspectos y desafíos: a) la factibilidad de identificar pacientes con sospecha de HF a través de la implementación de la pesquisa por oportunidad de esta patología; b) la oportunidad de realizar el estudio en cascada familiar a partir de la identificación de CI de HF, un método costo-efectivo de diagnóstico para patologías de origen genético 24, 25 ; c) la necesidad de contar con herramientas genéticas para el sistema de salud, que permitan el diagnóstico definitivo de HF en todas las personas con sospecha clínica de esta patología. Esta estrategia es costo efectiva 15, 26, al diagnosticar con certeza y tempranamente la patología, favoreciendo el estudio en cascada familiar.
En conclusión, este estudio representa un primer paso fundamental en la búsqueda de pacientes con Hipercolesterolemia Familiar en el sistema de salud chileno. Los hallazgos de este estudio piloto en el Hospital Las Higueras de Talcahuano evidencian la necesidad de la implementación de programas de pesquisa sistemáticos en instituciones de salud pública, con el objetivo de identificar y tratar a esta población altamente subdiagnosticada y de alto riesgo de ECV. A largo plazo, esta iniciativa podría contribuir a disminuir la morbilidad y mortalidad cardiovascular asociada a la IC en nuestro país. Sin embargo, se requieren estudios adicionales a mayor escala para confirmar estos antecedentes y evaluar el impacto a largo plazo de esta estrategia.
Financiamiento: Fondecyt de Iniciación N° 11220497; Vrid-Multidisciplinario 2021000299MUL Universidad de Concepción, Chile.
Encontrá más notas de esta sección aquí: https://revistabioreview.com/category/secciones/bioquimica-molecular/
REFERENCIAS BIBLIOGRÁFICAS
- Defesche JC, Gidding SS, Harada-Shiba M, Hegele RA, Santos RD, Wierzbicki AS. Hipercolesterolemia familiar. Imprimaciones Nat Rev Dis. 2017; 3: 17093.
- Mata P, Alonso R, Ruiz A, González-Juanatey JR, Badimon L, Díaz-Díaz JL, et al. Diagnóstico y tratamiento de la hipercolesterolemia familiar en España: Documento de consenso. Semergen. 2015; 41(1): 24-33.
- Lan NSR, Martin AC, Brett T, Watts GF, Bell DA. Mejora de la detección de la hipercolesterolemia familiar. Pathology. 2019; 51(2): 213-221.
- Di Taranto MD, Fortunato G. Heterogeneidad genética de la hipercolesterolemia familiar: repercusiones para el diagnóstico molecular. Int J Mol Sci. 2023; 24(4): 3224.
- Di Taranto MD, Giacobbe C, Fortunato G. Hipercolesterolemia familiar: una enfermedad genética compleja con fenotipos variables. Eur J Med Genet. 2020; 63(4): 103831.
- Cuchel M, Bruckert E, Ginsberg HN, Raal FJ, Santos RD, Hegele RA, et al. Hipercolesterolemia familiar homocigótica: Nuevos conocimientos y guía para clínicos para mejorar la detección y el manejo clínico. Documento de posición del Panel de Consenso sobre Hipercolesterolemia Familiar de la Sociedad Europea de Aterosclerosis. Eur Heart J. 2014; 35(32): 2146-2157.
- Beheshti SO, Madsen CM, Varbo A, Nordestgaard BG. Prevalencia mundial de la hipercolesterolemia familiar: metaanálisis de 11 millones de sujetos. J Am Coll Cardiol. 2020; 75(20): 2553-2566.
- Henderson R, O’Kane M, McGilligan V, Watterson S. Genética y cribado de la hipercolesterolemia familiar. J Biomed Sci. 2016; 23: 39.
- Seguro F, Bongard V, Berard E, Taraszkiewicz D, Ruidavets JB, Ferrieres J. Los criterios de colesterol de lipoproteínas de baja densidad de la Red Holandesa de Clínicas de Lípidos se asocian con la mortalidad a largo plazo en la población general. Arch Cardiovasc Dis. 2015; 108(10): 511-518.
- Organización. OMS. Hipercolesterolemia familiar: Informe de una segunda consulta de la OMS, Organización Mundial de la Salud, Programa de Genética Humana, División de Enfermedades No Transmisibles. Organización Mundial de la Salud, Ginebra, Suiza. 1999; publicación de la OMS n.º WHO7HGN/FH/CONS/99.2.
- Sanchez A, Bustos P, Honorato P, Saez K, Elim-Jannes C, Barriga N, et al. Identificación de variantes genéticas asociadas con hipercolesterolemia familiar en niños y adolescentes chilenos. Rev Med Chil. 2021; 149(9): 1267-1274.
- Salud Md. Orientación técnica dislipidemias. 2018.
- Bell DA, Hooper AJ, Bender R, McMahon J, Edwards G, van Bockxmeer FM, et al. Detección oportunista de hipercolesterolemia familiar mediante un laboratorio comunitario. Ann Clin Biochem. 2012; 49(Pt 6): 534-537.
- Mirzaee S, Choy KW, Doery JCG, Zaman S, Cameron JD, Nasis A. El laboratorio del hospital terciario: una nueva vía para la detección oportunista de la hipercolesterolemia familiar. Int J Cardiol Heart Vasc. 2019; 23: 100354.
- Gutiérrez-Cortizo EN, Romero-Jiménez MJ, Rodríguez MEM, Santos MAD, Granado FJC, Ruiz-Granados ES, et al. Detección de Hipercolesterolemia Familiar mediante datos analíticos centralizados. Programa HF huelva detecta. Endocrinol Diabetes Nutr (Ed. Inglesa). 2021; 68(7): 450-457.
- Representantes de la C Global de Hipercolesterolemia Familiar, Wilemon KA, Patel J, Aguilar-Salinas C, Ahmed CD, Alkhnifsawi M, et al. Reducción de la carga clínica y de salud pública de la hipercolesterolemia familiar: un llamado global a la acción. JAMA Cardiol. 2020; 5(2): 217-229.
- Mata P, Alonso R, Pérez-Jiménez F. Detección de hipercolesterolemia familiar: Un modelo para la medicina preventiva. Rev Esp Cardiol (Ed. en inglés). 2014; 67(9): 685-688.
- Nordestgaard BG, Chapman MJ, Humphries SE, Ginsberg HN, Masana L, Descamps OS, et al. La hipercolesterolemia familiar está infradiagnosticada e infratratada en la población general: Guía para clínicos para la prevención de la cardiopatía coronaria: Declaración de consenso de la Sociedad Europea de Aterosclerosis. Eur Heart J. 2013; 34(45): 3478-90a.
- Salud Md. Encuesta Nacional de Salud 2016-2017: https://redsalud.ssmso.cl/wp-content/uploads/2018/02/2-Resultados-ENS_MINSAL_31_01_2018-ilovepdf-compressed.pdf
- Tokgozoglu L, Kayikcioglu M. Hipercolesterolemia familiar: carga global y enfoques. Curr Cardiol Rep. 2021; 23(10): 151.
- Lelli N, Ghisellini M, Calandra S, Gaddi A, Ciarrocchi A, Coviello DA, et al. Duplicación de los exones 13, 14 y 15 del gen del receptor de LDL en un paciente con hipercolesterolemia familiar heterocigota. Hum Genet. 1991; 86(4): 359-362.
- Wiegman A, Gidding SS, Watts GF, Chapman MJ, Ginsberg HN, Cuchel M, et al. Hipercolesterolemia familiar en niños y adolescentes: Ganar décadas de vida optimizando la detección y el tratamiento. Eur Heart J. 2015; 36(36): 2425-2437.
- Ascaso JF, Mata P, Arbona C, Civeira F, Valdivielso P, Masana L. Hipercolesterolemia familiar homocigótica: adaptación española del documento de consenso del Panel de Consenso sobre Hipercolesterolemia Familiar de la Sociedad Europea de Aterosclerosis. Documento de consenso de la Sociedad Española de Arteriosclerosis (SEA) y la Fundación de Hipercolesterolemia Familiar (FHF). Clin Investig Arterioscler. 2015; 27(2): 80-96.
- Lazaro P, Perez de Isla L, Watts GF, Alonso R, Norman R, Muniz O, et al. Rentabilidad de un programa de cribado en cascada para la detección precoz de la hipercolesterolemia familiar. J Clin Lipidol. 2017; 11(1): 260-271.
- Gidding SS, Sheldon A, Neben CL, Williams HE, Law S, Zhou AY, et al. Aceptación por parte de los pacientes de las pruebas genéticas para la hipercolesterolemia familiar en el Registro CASCADE FH. J Clin Lipidol. 2020; 14(2): 218-23 e2.
- Arrobas Velilla T, Brea A, Valdivielso P, los investigadores del Proyecto A, Investigadores del proyecto ARA. Implantación de un programa de cribado bioquímico y genético para la hipercolesterolemia familiar. Colaboración entre el laboratorio clínico y las unidades de lípidos: Diseño del Proyecto ARIAN. Clin Investig Arterioscler. 2021; 33(6): 289-295.
- Hipercolesterolemia familiar: Identificación y manejo: Revisiones de la evidencia para la detección de casos, el diagnóstico y la monoterapia con estatinas. Colección de revisiones de la evidencia del NICE. Londres 2017.
- Recibido: 7 de marzo de 2024; Aceito: 20 de marzo de 2025. Los autores declaran no tener conflicto de intereses.
- Licencia Creative Commons: Este es un artículo de acceso abierto distribuido bajo los términos de la Licencia Creative Commons Atribución, que permite el uso, la distribución y la reproducción sin restricciones en cualquier medio, siempre que se cite correctamente la obra original.







