
Quidel Triage® Profiler SOB TM Panel: como hallar la causa de una disnea en solo 20 minutos
La dificultad respiratoria (disnea) es una causa frecuente de visita a las salas de urgencias. Es un síntoma inespecífico cuya causa puede ser de alto riesgo, como en el caso del infarto agudo de miocardio (IAM), insuficiencia cardiaca (IC) o embolia pulmonar (EP). La disnea abarca una variedad de sensaciones desagradables relacionadas con la respiración, … Quidel Triage® Profiler SOB TM Panel: como hallar la causa de una disnea en solo 20 minutos

La dificultad respiratoria (disnea) es una causa frecuente de visita a las salas de urgencias. Es un síntoma inespecífico cuya causa puede ser de alto riesgo, como en el caso del infarto agudo de miocardio (IAM), insuficiencia cardiaca (IC) o embolia pulmonar (EP).
La disnea abarca una variedad de sensaciones desagradables relacionadas con la respiración, incluidas la falta de aire y la sensación de trabajo, esfuerzo u opresión en el pecho. Puede variar en intensidad según el mecanismo fisiopatológico involucrado, y su percepción está influenciada por las características sociales, culturales y psicológicas del paciente1.
El diagnóstico diferencial de la condición causal es complejo debido a su falta de especificidad y a la asociación pobre entre su intensidad y la gravedad de la patología subyacente. En el estudio inicial de una disnea, por lo tanto, es fundamental una evaluación diagnóstica rápida que aporte información útil para asignar al paciente al entorno de atención más adecuado, permitiendo establecer una estrategia de tratamiento y seguimiento óptima2.
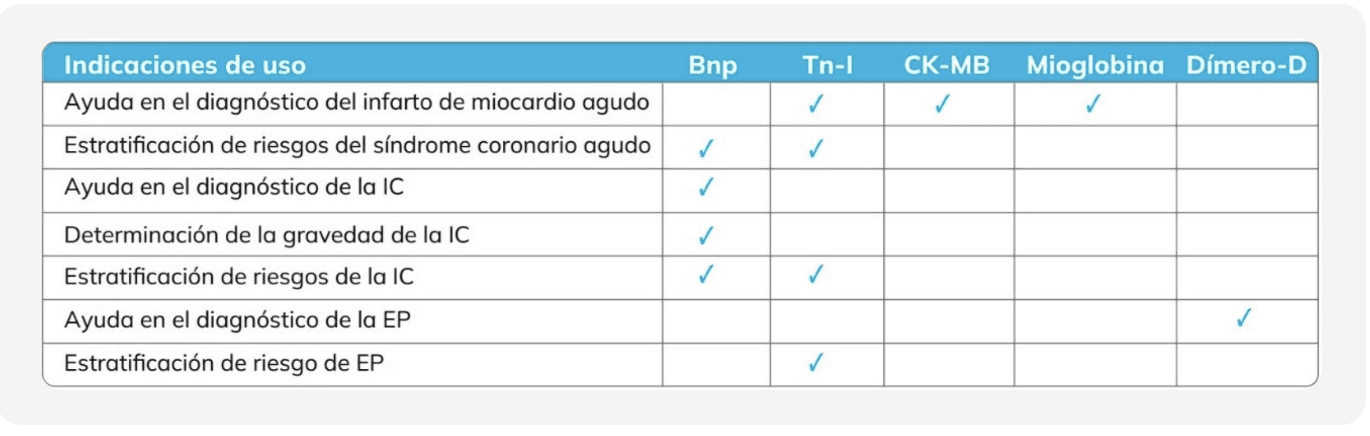
Desde el laboratorio de urgencias existen distintos parámetros que pueden ayudar a identificar la causa de la disnea y que permiten clasificar a los pacientes según el riesgo de desarrollar una condición grave. Los siguientes parámetros son recomendados para la evaluación inicial:
Péptido natriurético tipo B (BNP): En sus directrices, la Sociedad Europea de Cardiología establece los umbrales de ≥ 100 pg/mL para el BNP y ≥ 300 pg/mL para el péptido natriurético tipo B pro-N-terminal (NT-proBNP), excluyendo valores inferiores una insuficiencia cardíaca aguda3.
Troponinas cardíacas: la lesión miocárdica, definida por un valor elevado de troponina cardíaca (cTn), se asocia con un pronóstico adverso. Las troponinas cardíacas I (cTnI) y T (cTnT) se expresan casi exclusivamente en el corazón. No se ha informado que se produzcan aumentos en los valores de cTnI después de una lesión en tejidos no cardíacos; en cambio, el músculo esquelético lesionado expresa proteínas que se detectan mediante algunos ensayos para cTnT, lo que conduce a algunas situaciones en las que las elevaciones de cTnT podrían ser no específicas de una lesión miocárdica4. Por otra parte, el nivel de elevación de cTn puede ser indicativo del tamaño de la lesión5.
Creatina quinasa MB (CK-MB): por lo general, la elevación de la CK-MB es detectable dentro de las primeras 12 horas luego del inicio de un IAM. Si bien puede elevarse también como consecuencia de daño muscular agudo o crónico, la determinación de su concentración en sangre sigue siendo una herramienta fiable para el diagnóstico y tratamiento de los pacientes con IAM. Además, el análisis de los niveles máximos de CK-MB también puede ser útil para estimar el tamaño del infarto y predecir disfunción ventricular izquierda6.
Mioglobina: a pesar de no tener tanta especificidad, la mioglobina sérica aumenta en un período de 1 a 4 horas y es más sensible durante este período temprano que otros marcadores7. Es por esto que posee su mayor valor en la exclusión del IAM en las primeras horas después del dolor torácico, y es particularmente útil cuando se conocen los antecedentes clínicos del paciente.
Dímero D: se han descrito aumentos de la concentración de dímero D circulante en pacientes con tromboembolia venosa, incluida la embolia pulmonar (EP) y la trombosis venosa profunda (TVP).
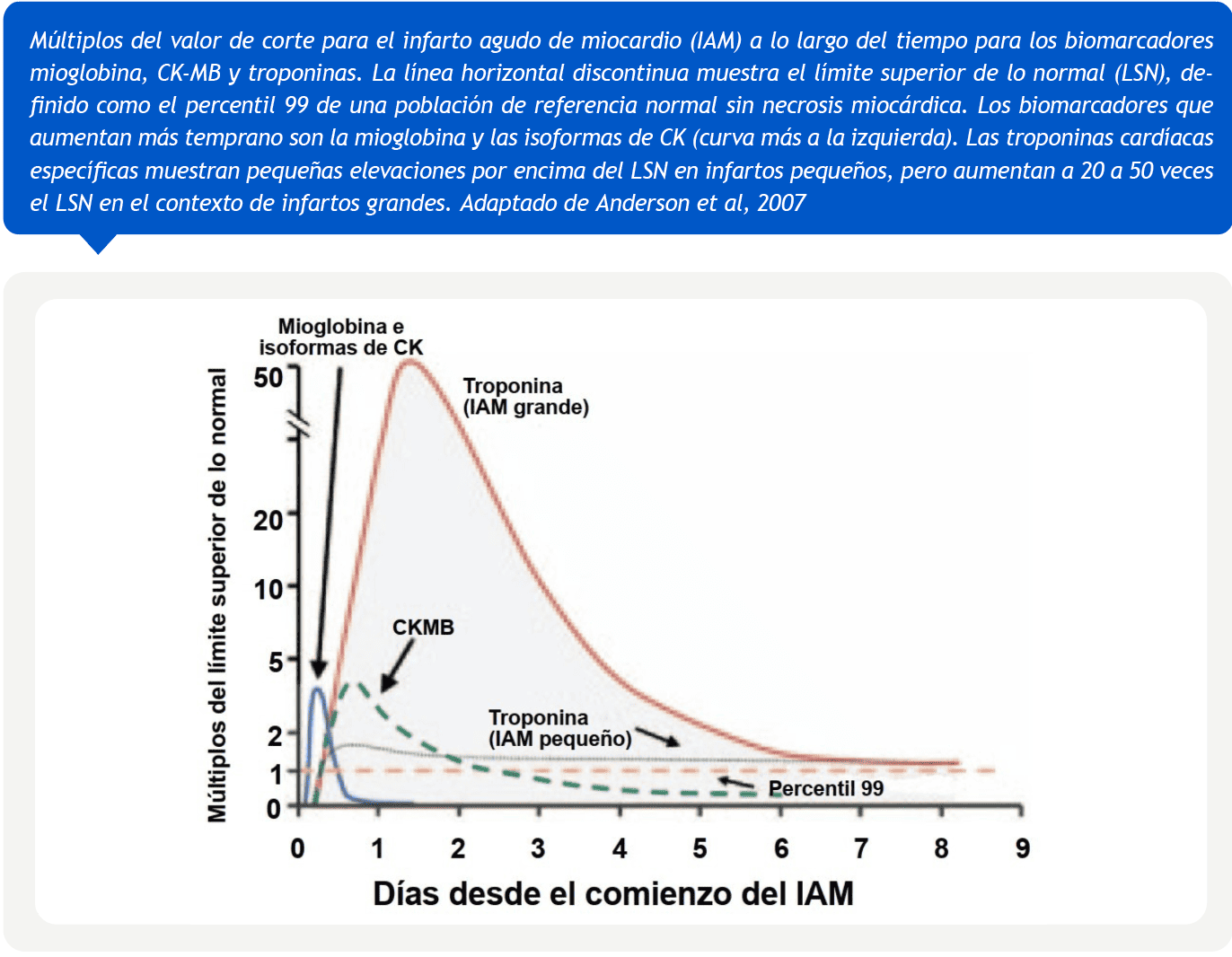
Un enfoque multiparamétrico, entonces, identifica rápidamente a los pacientes con un IAM y proporciona una mejor estratificación del riesgo de mortalidad que el análisis de un solo marcador8.
Quidel Triage® Profiler SOB™ Panel es un inmunoensayo de fluorescencia que permite distinguir entre causas de disnea de forma rápida. El panel se utiliza con el instrumento Quidel Triage MeterPro, completamente portátil, obteniéndose resultados cuantitativos simultáneamente para mioglobina, CK-MB, troponina I, BNP y dímero D.
A diferencia de otras pruebas convencionales, que pueden demorar horas, Quidel Triage Profiler SOB Panel proporciona resultados para los 5 marcadores en tan solo 20 minutos. Esto permite una toma de decisiones más rápida, mejorando así las expectativas para el paciente al poderle brindar un tratamiento adecuado. Además, al permitir un diagnóstico temprano preciso, contribuye a la optimización de recursos en los centros de salud.
Con un diagnóstico claro, se puede evitar la hospitalización innecesaria de pacientes con condiciones menores y redirigir los recursos hacia aquellos que requieren atención urgente y especializada.
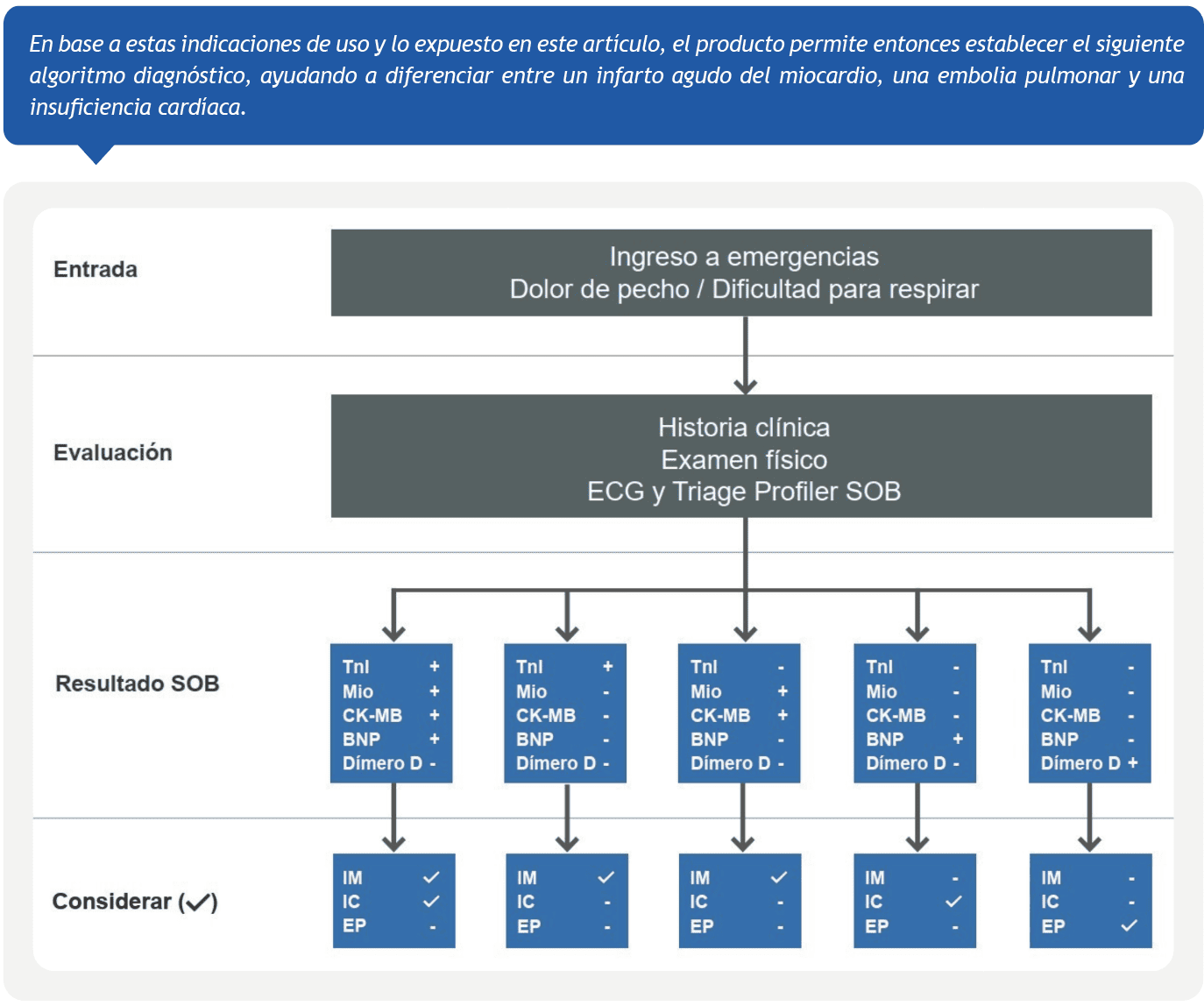
Por todo esto, Quidel Triage® Profiler SOB™ Panel, en contextos de urgencia, es una herramienta invaluable en entornos de alta demanda.
Sólo 3 simples pasos:
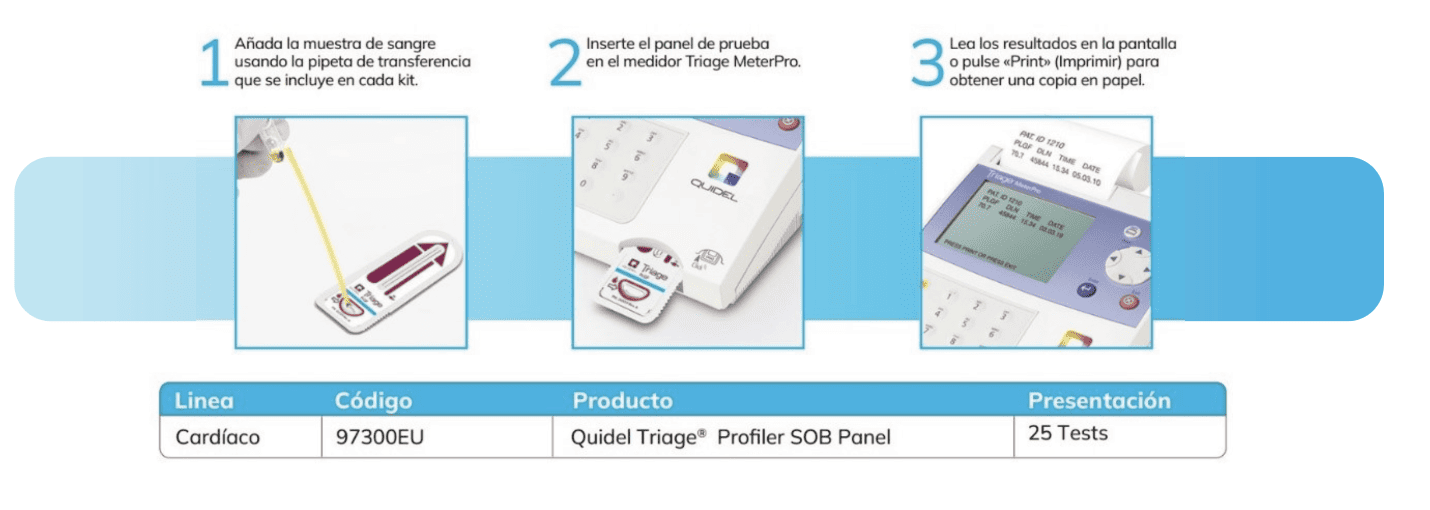
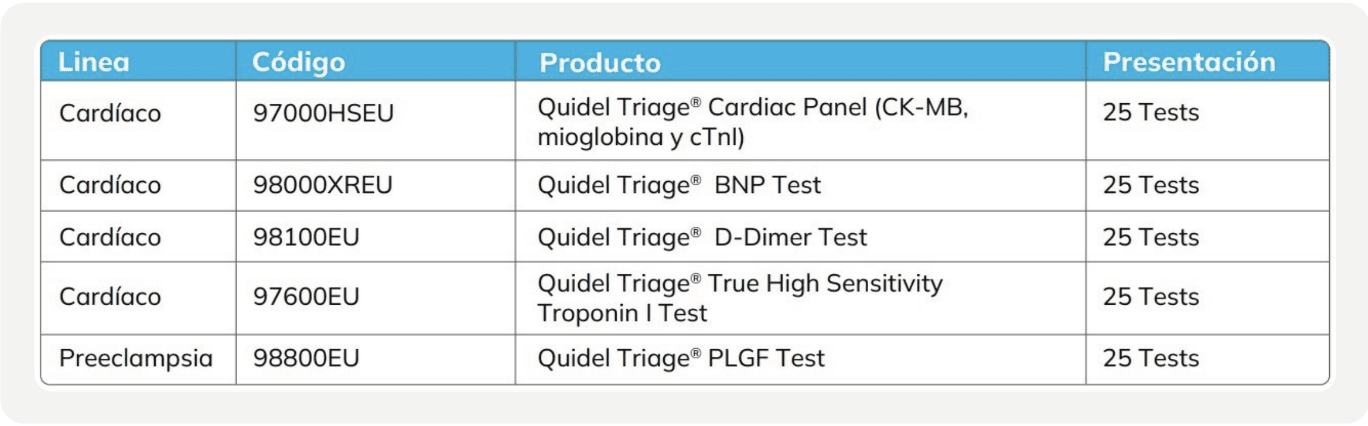
También disponibles para Quidel Triage®:
Referencias Bibliográficas
1. Santus, P. et al. Acute dyspnea in the emergency department: a clinical review. Internal and Emergency Medicine vol. 18 1491–1507 Preprint at https://doi.org/10.1007/s11739-023-03322-8 (2023).
2. Parshall, M. B. et al. An official American thoracic society statement: Update on the mechanisms, assessment, and management of dyspnea. American Journal of Respiratory and Critical Care Medicine vol. 185 435–452 Preprint at https://doi.org/10.1164/rccm.201111-2042ST (2012).
3. McDonagh, T. A. et al. 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. European Heart Journal vol. 42 3599–3726 Preprint at https://doi.org/10.1093/eurheartj/ehab368 (2021).
4. Thygesen, K. et al. Fourth Universal Definition of Myocardial Infarction (2018). J Am Coll Cardiol 72, 2231–2264 (2018).
5. Anderson, J. L. et al. ACC/AHA 2007 guidelines for the management of patients with unstable angina/non ST-elevation myocardial infarction: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Writing Committee to Revise the 2002 Guidelines for the Management of Patients With Unstable Angina/Non ST-Elevation Myocardial Infarction): developed in collaboration with. Circulation 116, (2007).
6. Alnemer, K. A. In-Hospital Mortality in Patients With Acute Myocardial Infarction: A Literature Overview. Cureus (2024) doi:10.7759/cureus.66729.
7. Harrison, A. & Amundson, S. Evaluation and management of the acutely dyspneic patient: The role of biomarkers. American Journal of Emergency Medicine 23, 371–378 (2005).
8. Newby, L. K. et al. Bedside Multimarker Testing for Risk Stratification in Chest Pain Units The Chest Pain Evaluation by Creatine Kinase-MB, Myoglobin, and Troponin I (CHECKMATE) Study. Circulation vol. 103 http://www.circulationaha.org (2001)





