
Hepatitis C
Las recomendaciones internacionales para el estudio de anticuerpos anti-HCV ha ido modificándose en los últimos años y así dan cuentan las publicadas en 1998, 2003 y 2012, esta última incorporando el estudio por una única vez de anti-HCV para personas nacidas entre 1945-1965 (1,2,3,4). En el mismo sentido los ensayos serológicos, moleculares y los respectivos algoritmos de diagnóstico también han ido modificándose permitiendo un diagnóstico mucho más preciso.
María Belen Bouzas, María Eugenia Garay,Diego Arrigo
Artículo en evaluación del Libro de Resúmenes del Consenso Argentino de Hepatitis 2013
Asociación Argentina para el Estudio de las Enfermedades de Hígado
Parte B
Fabian Fay, Beatriz Libellara, Rodolfo Campos
Artículo en evaluación del Libro de Resúmenes del Consenso Argentino de Hepatitis 2013
Asociación Argentina para el Estudio de las Enfermedades de Hígado
Parte C
Silvia Paz, Raul Adrover, Ariel Ramadan
Artículo en evaluación del Libro de Resúmenes del Consenso Argentino de Hepatitis 2013
Asociación Argentina para el Estudio de las Enfermedades de Hígado
A. Diagnóstico serológico
Las recomendaciones internacionales para el estudio de anticuerpos anti-HCV ha ido modificándose en los últimos años y así dan cuentan las publicadas en 1998, 2003 y 2012, esta última incorporando el estudio por una única vez de anti-HCV para personas nacidas entre 1945-1965 (1,2,3,4). En el mismo sentido los ensayos serológicos, moleculares y los respectivos algoritmos de diagnóstico también han ido modificándose permitiendo un diagnóstico mucho más preciso. En virtud de los cambios en la disponibilidad de ensayos para la detección de anti-HCV, los avances en el desarrollo de antivirales y considerando que aún personas identificadas como anti-HCV positivas no son posteriormente evaluadas para establecer su condición de infección, es necesario establecer algoritmos simples que mejoren la accesibilidad al diagnóstico, siendo a la vez más eficientes.
Ensayos de Tamizaje
Los enzimoinmunoensayos (EIE) de segunda (2G) y tercera (3G) generación generalmente detectan una mezcla de anticuerpos de tipo IgG anti HCV contra varios epitopes del core, NS3 y NS4, estas modificaciones mejoraron marcadamente la sensibilidad y especificidad de los mismos. La diferencia entre ambas generaciones de ensayos es la incorporación de un antígeno adicional de la región NS5 (5,6). La presentación de estos ensayos puede ser manual, semiautomática o totalmente automática y en la mayoría de ellos los antígenos empleados son proteínas recombinantes. La reducción de la ventana serológica en estos ensayos es de un promedio de 5 semanas en comparación con los de primera generación, permitiendo la detección de anticuerpos hasta 10 semanas post-exposición. La especificidad de los EIE 3G excede el 99%, observándose falsos negativos en pacientes en hemodiálisis o inmunosuprimidos (7). En poblaciones con prevalencias de infección inferiores al 10% estos EIE pueden tener valores predictivos positivos bajos (1).
Inmunoensayos para Ag Core de HCV
Se encuentran disponibles ensayos que tienen la capacidad de detectar antígeno de core solamente o bien la combinación con anticuerpos, denominados ensayos combinados (combos), estos últimos de poca aceptabilidad en laboratorios clínicos (8,9). En el caso de los primeros, ha demostrado tener una sensibilidad entre el 80-90% y una especificidad entre el 96-100% en el periodo de ventana. Si bien la sensibilidad es equivalente para todos los genotipos la detección de fenotipo 1 es mejor que para el 3, y la sensibilidad es menor que la de los de testeo de ácidos nucleicos (TAN) (10,11)
Ensayos suplementarios
Dentro de los ensayos suplementarios se incluyen aquellos que son serológicos para anti-HCV (de mayor especificidad que los ensayos de tamizaje) y aquellos que detectan ácidos nucleicos (TAN) (12,13). En el caso de los primeros, se trata de un inmunoblot que emplea antígenos recombinantes y/o péptidos sintéticos de la región del core, NS3 y NS5. Los resultados obtenidos en los ensayos serológicos suplementarios son interpretados como positivo, indeterminado, o negativo de acuerdo al número de bandas presentes o ausencia de las mismas respectivamente. Se trata de una determinación costosa y laboriosa en su procedimiento. Puede tener falsos negativos al inicio de la infección, en pacientes inmunocomprometidos o en pacientes que hayan resuelto la infección, y la confirmación de un resultado positivo no confirma la infección presente (14). En la actualidad y en nuestro país, se encuentra comercialmente disponible solo LIA HCV (Innogenetics). Dentro de los métodos TAN se encuentran aquellos que lo hacen en forma cualitativa o cuantitativa como se describe en el artículo siguiente. La especificidad reportada para algunos de estos ensayos se encuentra entre 98-99%. Su aplicación es cada vez mayor en el diagnóstico, ya que en la actualidad además de ser utilizados en el diagnóstico de la hepatitis aguda el mismo se encuentra incorporado en el algoritmo de diagnóstico (15).
Nuevos métodos disponibles: Tests Rápidos
Los dispositivos rápidos comúnmente denominados test rápidos se caracterizan por ser simples y rápidos, no requieren de equipamiento sofisticado para su realización y el resultado puede obtenerse entre los 4-30 minutos. Poseen la ventaja de requerir pequeños volúmenes para su realización, y se encuentran estandarizados para sangre entera y saliva. En todos los casos se trata de métodos inmunocromatográficos, cuya presentación puede ser cassette, cartucho o tarjeta. La sensibilidad reportada varía entre 86%-99% con una especificidad superior al 99%. En la actualidad la FDA ha aprobado uno de ellos (OraQuick) para individuos >15 años con riesgo de infección o personas con signos y síntomas de hepatitis (16). Se han desarrollado comercialmente ambién tests rápidos que detectan simultáneamente anticuerpos o antígenos para sífilis, HIV y HBV. En nuestro país aún no hay datos publicados sobre la performance de los mismos pero estos ensayos pueden llegar a tener un alto impacto en términos de accesibilidad al diagnóstico y tratamiento oportuno.
Algoritmo de diagnóstico
Los algoritmos diagnósticos también han ido modificándose en los últimos años. Realizar el testeo suplementario reflejo (Reflex) inicialmente era complejo, costoso y tenía un tiempo extendido en la devolución del resultado (2). Este fue seguido posteriormente por una serie de guías que incluían el uso de cortes de positividad (RP, s/co), específicos para cada ensayo, a partir del cual el valor predictivo de un resultado positivo es >95% (2, 16,17). La mayoría de los ensayos evaluados con sus respectivos cortes incluye equipos automáticos con lo cual para muchos ensayos manuales no se encuentran disponibles esos valores, convirtiéndose en una limitante al momento de la aplicación de este algoritmo (tabla de valores, paper cortes). La secuencia recomendada comienza con un ensayo de laboratorio para anti-HCV, si el mismo fuera No Reactivo e indica que anti-HCV no es detectado.
Un resultado Reactivo puede indicar: 1) infección presente, 2) infección pasada o 3) falso positivo.
Un resultado reactivo debe ser seguido por la detección de TAN para HCV-RNA. Un resultado de HCV-RNA Detectable indica Infección Presente y un resultado de HCV-RNA No Detectable indica Infección Pasada o eventual Falso Positivo. Si se quisiera diferenciar entre estas dos últimas situaciones, un segundo ensayo para anti-HCV puede incorporarse ya que dado que los antígenos, plataformas y performance de los ensayos varía es poco probable que una falsa reacción se observe en dos ensayos distintos (Tabla 1- a ver a la derecha). En este algoritmo no es necesario que el resultado reactivo sea reportado con su relación de positividad, y es importante resaltar que en estas recomendaciones es indistinto si el ensayo de tamizaje es por un método de laboratorio o si es a partir de un test rápido (15).
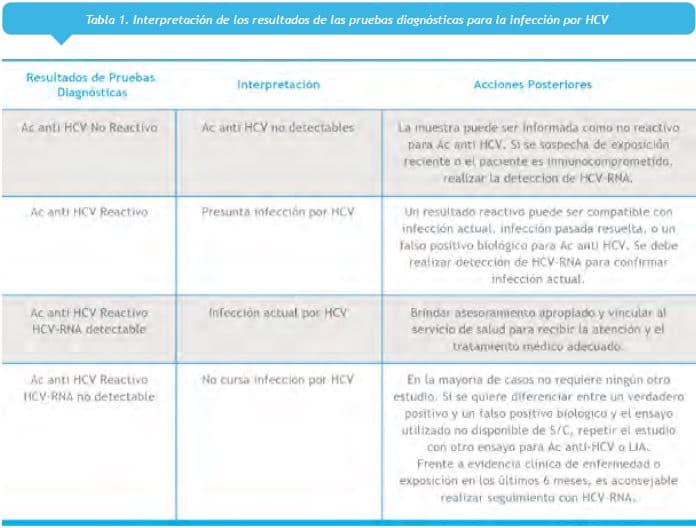
Recomendaciones respecto toma de muestra y transporte
La muestra de elección tanto para serología como para biología molecular es la de suero colectado preferente Tabla 1. Interpretación de los resultados de las pruebas diagnósticas para la infección por HCV en tubos con gel separador. La muestra para la detección molecular debe ser obtenida de un tubo independiente del empleado para serología, y en todos los casos correctamente identificado.
El transporte a los centros receptores o de referencia debe ser dentro de bolsas de transportes de bioseguridad colocados dentro de recipiente secundario y terciario respectivamente, con su correspondiente solicitud de pedido en compartimento separado.
B. Biología molecular. Utilidad en el diagnóstico y en la evaluación de la respuesta al tratamiento
Los métodos de biología molecular aplicables al diagnóstico y evaluación de la respuesta al tratamiento de la Hepatitis C a la fecha son los que se detallan a continuación:
• Detección de HCV-RNA cualitativo en suero/plasma.
• Detección de HCV-RNA cuantitativo (Carga Viral) en suero/plasma.
Deteccion de HCV-RNA cualitativo en suero o plasma
Los métodos cualitativos detectan el HCV-RNA en plasma/suero y arrojan un resultado DETECTABLE /NO DETECTABLE. Se basan en reacciones de amplificación por PCR dirigidas hacia la región 5’NC. Solo son aplicables métodos comerciales.
Aplicaciones:
- Confirmar replicación viral en pacientes con Anticuerpos anti- Hepatitis C.
- Determinación de infección por HCV en pacientes inmunosuprimidos.
- Definición de infección por HCV en recién nacidos de madres portadoras de HCV.
- Definición de infección por HCV en casos compatibles con infección HCV aguda.
- Detección de HCV-RNA en sangre y hemoderivados.
El detalle de los test comerciales disponibles y su sensibilidad se detallan en la Tabla 1-b (ver a la derecha).
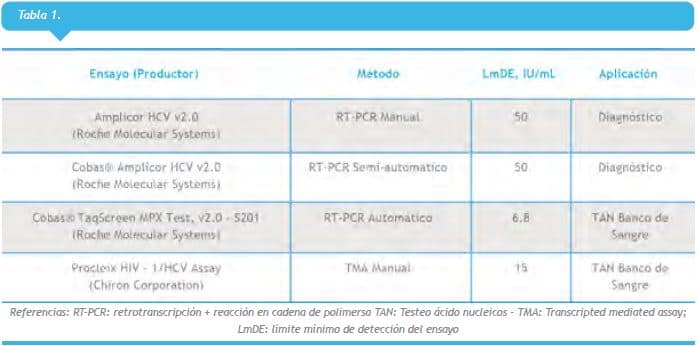
Cómo debe informarse un método cualitativo
Método: especificar Ensayo y marca comercial Límite mínimo de detección del ensayo (LmDE)= expresado en UI/mL.
Resultados: Detectable / No detectable
Detección de HCV-RNA cuantitativo (Carga Viral) en suero/plasma.
Los métodos cuantitativos detectan y cuantifican el nivel de HCV-RNA en plasma/suero. Sus métodos se basan en amplificaciones por PCR en tiempo real. Solo son aplicables métodos comerciales que expresen sus resultados en UI/mL.
Aplicaciones
Determinar los valores de carga viral antes del inicio del tratamiento, durante el mismo y en el seguimiento.
Es una herramienta fundamental para la toma de decisiones terapéuticas, sobre todo en el contexto de las nuevas drogas, ya que de su resultado se definen la terapia guiada por la respuesta y las reglas de inutilidad.
Es importante hacer notar que las últimas versiones disponibles (*1 en la tabla) su sensibilidad es superior a los test cualitativos con lo cual su uso puede reemplazar o desplazar al test cualitativo, utilizándose la carga viral como test confirmatorio de la infección por HCV.
Los métodos comerciales disponibles y sus características se detallan en la Tabla 2 (ver a la derecha).
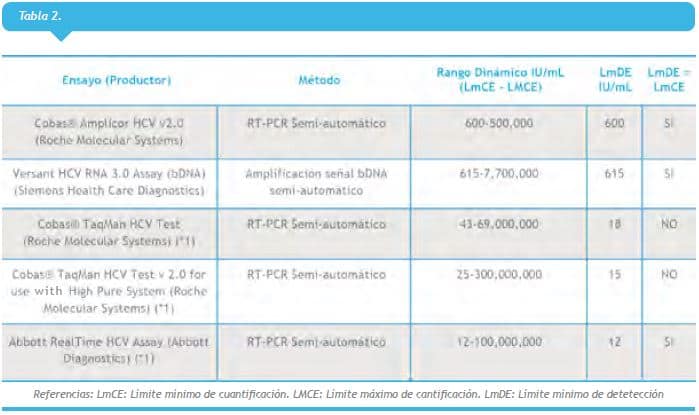
Solo los métodos (*1) son utilizables en el contexto de los nuevos tratamientos ya que se requieren sensibilidad menor o igual a 25 UI/mL. Algunos métodos presentan límites de cuantificación y de detección diferentes. Para su uso en el contexto de los nuevos tratamientos, un resultado detectable no cuantificable, entre el límite de cuantificación (25 UI/mL) y el límite de detección (15 UI/mL) debe considerarse positivos para la toma de decisiones sobre respuesta temprana, suspensión de tratamiento, o reactivación post-suspensión del tratamiento.
Valores superiores al límite máximo de cuantificación no requieren diluciones en función de que los nuevos esquemas plantean requerimientos de disminución de la carga viral que no están relacionados con el valor inicial del tratamiento.
Se recomienda que siempre se mida la carga viral con el mismo método y en lo posible en el mismo laboratorio. Asimismo, se recomiendan a los laboratorios que realicen estos ensayos que estén suscritos a programas de control de calidad o que tengan acreditadas esta técnica ante requisitos internacionales (CAP – ISO 15189).
Cómo debe informarse un método cuantitativo
Método: especificar Ensayo y marca comercial
Rango dinámico del ensayo: LmCE (límite mínimo de cuantificación) – LMCE (límite máximo de cuantificación).
Límite mínimo de detección del ensayo (LmDE)= expresado en UI/mL (*2).
Resultados: Detectable / Detectable no cuantificable /No detectable.
Valor hallado: Resultado expresado en UI/mL (solo en resultados detectables) (*2): este valor debe ser comprobado e informado por el laboratorio.
C. ¿En quiénes se debe investigar el HCV? Ventajas y desventajas del screening universal
La hepatitis C es una causa creciente de morbilidad y mortalidad en el mundo. Durante muchos años, la terapéutica de la hepatitis C se vio limitada al uso de Interferon Pegilado y Ribavirina, con pobres resultados especialmente para el genotipo más frecuente (genotipo 1), además de los efectos adversos conocidos y las limitantes que plantea el uso de Interferón en aquellos pacientes con comorbilidades o cirrosis descompensada.Sin embargo, en los últimos tiempos, estamos asistiendo a un cambio radical en la terapéutica, con el desarrollo de nuevas drogas, los antivirales de acción directa.
Estas drogas, no solo aumentan la posibilidad de respuesta al tratamiento y consecuente curación, sino que lo hacen con menos efectos adversos y más fácil posología. Además, los nuevos tratamientos ampliaran el universo de pacientes pasibles de ser tratados ya que se encuentran en desarrollo terapias libres de Interferón.
La hepatitis C es una enfermedad crónica que es principalmente diagnosticada de forma casual, dado que es asintomática en la mayoría de los casos. Esto implica el desconocimiento de la enfermedad por un importante número de pacientes (1). En Estados Unidos, se calcula que un 50% de las personas infectadas con el virus C desconoce su diagnóstico (2,3). Un estudio europeo muestra que en Francia, el 44% de los infectados por HCV desconoce su condición, en Inglaterra el 69%, en el norte de España alcanza el 84%, en Alemania el 90% y en Polonia el 98% (4). Siendo que las consecuencias de la infección crónica pueden ser devastadoras (cirrosis, insuficiencia hepática, hepatocarcinoma) y que el desconocimiento ayuda a la diseminación de la enfermedad, es necesaria la búsqueda activa de la infección por virus C.
Según datos del CDC, solo un 55% de las personas infectadas por el virus C reportan factores de riesgo para la exposición al virus, siendo que el 45% restante desconoce la fuente de la enfermedad (5).
Se consideran factores de riesgo para adquirir la infección por virus C:
- Uso de drogas endovenosas,
- Transfusiones de sangre y derivados previas a 1992
- Hemodiálisis
- Uso de drogas inhalatorias
- Trabajadores de la salud
- Procedimientos invasivos
- Antecedentes de internaciones
- Conviviente de paciente con hepatitis C crónica
- Niños nacidos de madres con hepatitis C crónica
- Pareja sexual de paciente con hepatitis C crónica
- Hombres que tiene sexo con hombres
- Múltiples parejas sexuales
- Personas infectadas con HIV
En Estados Unidos se halló un riesgo 5 veces mayor de estar infectado con el virus de la hepatitis C en aquellos nacidos entre 1945 y 1964 (6), lo cual reflejaría las repetidas exposiciones percutáneas de esta población entre los años´70 y´80. No existen datos que homologuen la situación de nuestro país a la descripta para Estados Unidos. Resultados de la campaña “Dos semanas para cuidar tu hígado” llevada a cabo en el Hospital F. J. Muñiz en julio de 2012 muestran una prevalencia del 3.09% de anti-HCV reactivo en el total de la población estudiada y un 2.52% en aquellos nacidos entre 1945 y 1965. Sin embargo, sí puede decirse que la población de mayor edad ha estado expuesta a prácticas inseguras previas al uso de material descartable y las modernas técnicas de esterilización, así como a transfusiones de hemoderivados previo a 1992.
La estrategia de testear solo a aquellos con factores de riesgo ha tenido un éxito relativo, dado que, como se mencionó, aún permanece un gran número de pacientes sin diagnóstico. En la campaña antes mencionada, se diagnosticó un estadio de fibrosis avanzada (por elastografía hepática, Fibroscan R) en el 74% de las personas con anti HCV reactivo.
Es por ello, que la estrategia de testear a toda la población para la detección de hepatitis C al menos una vez en la vida puede resultar beneficiosa, dado que posibilitaría:
- Modificar conductas para evitar la transmisión
- Corregir factores como el consumo de alcohol y el sobrepeso
- Testeo y vacunación de otras hepatitis virales
- Acceso al cuidado y eventual tratamiento médico
- Prevenir el desarrollo de complicaciones (7,8)
En conclusión, dado que el testeo dirigido a las consideradas poblaciones de riesgo no puede ser considerado exitoso por el alto número de pacientes no diagnosticados y dado que contaremos progresivamente con mayores posibilidades de ofrecer un tratamiento curativo, es necesario ampliar el testeo de hepatitis C a toda la población, al menos una vez en la vida. Para lograr este objetivo, es necesario comprometer y educar a los profesionales de la salud de las áreas de la medicina con más contacto con la población considerada “sana” (clínicos, generalistas, pediatras, obstetras, ginecólogos), dado que deberán ser los que soliciten el test.
Las desventajas que plantea esta estrategia son exclusivamente económicas pero a corto plazo, dado que a largo plazo, los beneficios de diagnosticar (9) y tratar tempranamente la hepatitis C (10,11), previo al desarrollo de complicaciones, supera el costo de tratamiento de cirrosis descompensada, hepatocarcinoma y trasplante hepático, considerando no solo el costo de estos tratamientos (paliativos en muchos casos) sino también la disminución de la productividad de los pacientes afectados por estas patologías.
Referencas Bibliográficas
Parte A
1. CDC Recommendations for prevention and control of Hepatitis C virus (HCV) infection and HCV-related chronic disease . MMWR 1998,47 (No.RR19): 1—33.
2. CDC Guidelines for Laboratory testing and result reporting of antibody to Hepatitis C virus. MMWR, 2/7/03Vol2 (No RR3).
3. CDC. Recomendatios for the identification of Chronic hepatitis C virus infection among persons born during 945-1965. MMWR 2012; 61 (N0, RR4)
4. CDC Recommendation for prevention and control of Hepatitis C virus (HCV) infection and HCV-related chronic disease. MMWR/ May 7,2013/ VOL 62.
5. Rey J.A, Garcia M., Tomeo A., Arrayago A.,Ceriani S., Fernandez Toscano M., Insua M., Santamaria D., Kohan AI. Correlacion entre enzimoinmunoensayos anti HCV de segunda generacion y tercera generacion en donantes de sangre. Rev Arg Transf. 2000; 26 (1):41-4.
6. Colin C, LanoirD, Touzet S., Meyaud-Kraemer L., Bailly F., Trepo C. Sensisitivity and specificity of third- generation hepatitis C virus antibody detection assays: an analysis of the literature. J Viral Hepat 2001; 8:87-95.
7. Muerhoff AS, Jiang l., Shah Do, Gutierrez RA., Patel J., Garolis C., Kyrk CR., Leckie G., Frank A., Stewart JL., Dawson GJ.Detection of HCV core antigen in human serum or plasma with automated chemiluminescence analyzer. Transfusion 2002; 42: 349-56.
8. Gaudy C., Thevenas C. Usefulness of the Hepatitis C virus core antigen assay for screening of a population undergoing routine medical checkup. J Clin Microbiol ,April 2005, Vol3, N 4: 1722-1726.
9. Rivert A., Payan C., Morand B. Comparison of serum hepatitis C virus (HCV) RNA and core antigen levels in atients coinfected with human immunodeficiency virus and HCV and treated with interferon plus ribavirim J Clin Microbiol Feb 2006, Vol44, N2: 417-422.
10. Hosseini-Moghadam S., Iran Pur E., Rotstein C., Husain S., Lilly L., Renner E., Mazzulli T. Hepatitis C core Ag and its clinical applicability: potential advantages and disadvantages for diagnosis and follow-up?. Rev Med Virol May 2012; Vol 22, N3: 156-165.
11. Germer J., Zein N.N. Advances in molecular diagnosis of Hepatitis C and their clinical implications. Mayo Clin Proc. 2001; 76,911-920.
12. Dal Molin G., Tiribelli C,Campello C. A rational use of laboratory tests in the diagnosis and management of hepatitis C virus infection. Ann Hepatol 2003; 2(2)76-83.
13. Pawlotsky Jean Michel. Use and interpretation of Hepatitis C virus diagnostic assays. Clin Liver Dis 7 (2003), 127-137.
14. Chevaliez S., Pawlotsky J.M. Hepatitis C virus serologic and virologic tests and clinical diagnosis of HCV –related liver disease. Int J Med Sci 2006,3:35-40.
15. Testing for HCV infection: An update of guidance for clinicians and Laboratorians. MMWR/May 10, 2013/vol 62 No18: 362-365.
16. Saleem Kamili, Jan Drobeniuc, Aufra C. Araujo, and Tonya M. Hayden. Laboratory Diagnostics for Hepatitis C Virus Infection. CID 2012:55 (Supl 1).
17. Consenso Argentino de Hepatitis C2007. Asociacion Argentina para el estudio de las enfermedades del Higado. 27-29 Septiembre 2007.
Referencias Bibliográficas
Parte B
1. Ghany MG, Nelson DR, Strader DB, Thomas DL, Seeff LB; American Association for Study of Liver Diseases.An update on treatment of genotype 1 chronic hepatitis C virus infection: 2011 practice guideline by the American Association for the Study of Liver Diseases. Hepatology. 2011;54:1433-44.
2. Zitzer H, Heilek G, Truchon K, Susser S, Vermehren J, Sizmann D, Cobb B, Sarrazin C.
3. Second-generation Cobas AmpliPrep/Cobas TaqMan HCV quantitative test for viral load monitoring: a novel dual-probe assay design. J Clin Microbiol. 2013 Feb;51(2):571-7. doi: 10.1128/JCM.01784-12. Epub 2012 Dec 12.
4. Pawlotsky JM. Treatment of hepatitis C: how will we use viral kinetics, response-guided therapy? Curr Gastroenterol Rep. 2013 Feb;15(2):309. doi: 10.1007/s11894-012-0309-x.
5. Jacobson IM, Marcellin P, Zeuzem S, Sulkowski MS, Esteban R, Poordad F, Bruno S, Burroughs MH, Pedicone LD, Boparai N, Deng W, DiNubile MJ,Gottesdiener KM, Brass CA, Albrecht JK, Bronowicki JP. Refinement of stopping rules during treatment of hepatitis C genotype 1 infection with boceprevir and peginterferon/ ribavirin. Hepatology. 2012 Aug;56(2):567-75. doi: 10.1002/hep.25865. Epub 2012 Jun 29.
6. European Association for the Study of the Liver. 2011. EASL clinical practice guidelines: management of hepatitis C virus infection. J. Hepatol.55:245–264.
7. Ghany MG, Strader DB, Thomas DL, Seeff LB 2009. Diagnosis, management, and treatment of hepatitis C: an update. Hepatology49:1335–1374.
8. De Leuw P, Sarrazin C, Zeuzem S. 2011. How to use virological tools for the optimal management of chronic hepatitis C. Liver Int. 31(Suppl 1):3–12.
9. Cobb B, Vilchez RA . 2011. An update on treatment of hepatitis C virus genotype 1 and viral load assessments. Hepatology 55:979–980.
10. Harrington PR, Zeng W, Naeger LK. 2012. Clinical relevance of detectable but not quantifiable hepatitis C virus RNA during boceprevir or telaprevir treatment. Hepatology 55:1048–1057.
11. Chevaliez S . 2011. Virological tools to diagnose and monitor hepatitis C virus infection. Clin. Microbiol. Infect. 17:116–121.
12. Chevaliez S, Bouvier-Alias M, Pawlotsky JM. 2009. Performance of the Abbott real-time PCR assay using 2000sp and m2000rt for hepatitis C virus RNA quantification. J. Clin. Microbiol. 47:1726–1732.
13. Sarrazin C, Shiffman ML, Hadziyannis SJ, Lin A, Colucci G, Ishida H, Zeuzem S. 2010. Definition of rapid virologic response with a highly sensitive real-time PCR-based HCV RNA assay in peginterferon alfa-2a plus ribavirin response-guided therapy. J. Hepatol. 52:832–838.
14. Vermehren J, Colucci G, Gohl P, Hamdi N, Abdelaziz AI, Karey U, Thamke D, Zitzer H, Zeuzem S, Sarrazin C. 2011. Development of a second version of the Cobas AmpliPrep/ Cobas TaqMan hepatitis C virus quantitative test with improved genotype inclusivity. J. Clin. Microbiol. 49:3309–3315.
15. Vermehren J, Yu ML, Monto A, Yao JD, Anderson C, Bertuzis R, Schneider G, Sarrazin C. 2011. Multi-center evaluation of the Abbott RealTime HCV assay for monitoring patients undergoing antiviral therapy for chronic hepatitis C. J. Clin. Virol. 52:133–137.
16. European Association for the Study of the Liver. EASL Clinical Practice Guidelines: management of hepatitis C virus infection. J Hepatol. 2011;55:245-64.
17. Shiffman RN, Shekelle P, Overhage JM, Slutsky J, Grimshaw J, DeshpandeAM. Standardized reporting of clinical practice guidelines: a proposal from the Conference on Guideline Standardization. Ann Intern Med 2003;139:493-498.
Referencias Bibliográficas
Parte C
1. Roblin D, Smith B, Weinbaum C, Sabin M. Hepatitis C virus screening practices and prevalence in a managed care organization. Am J Managed Care 2011;17:548–55.
2. Gordon F. Cost-effectiveness of screening for hepatitis C.Am J Med. 1999;107:36S-40S.
3. Culver D, Alter M, Mullan R, Margolis H. Evaluation of the effectiveness of targeted lookback for HCV infection in the United States. Transfusion. 2000;40:1176-1181.
4. Eurasian Harm Reduction Network. Comparative analysis of HCV prevalence across selected countries of Europe and the Mediterranean area. October 2007.
5. CDC, datos no publicados, 2012
6. Smith B, Patel N, Beckett G, Jewett A. Hepatitis C virus antibody prevalence, correlates and predictors among persons born from 1945 through 1965, United States, 1999–2008 [Abstract]. American Association for the Study of Liver Disease, November 6, 2011. San Francisco, CA 2011.
7. Ghany M, Strader D, Thomas D, Seeff L. American Association for the Study of Liver D. Diagnosis, management, and treatment of hepatitis C: an update.
8. Poynard T. Hepatitis C: natural history, biology, treatment monitoring. Pathologie et biologie 1999;47:911–6.
9. Phillip C, Coffin O, John D, Scott M. Cost-effectiveness and Population Outcomes of General Population Screening for Hepatitis C. Clin Infect Dis. (2012) 54 (9): 1259-1271
10. Camma C, Petta S, Enea M, Bruno R. Cost-effectiveness of boceprevir or telaprevir for untreated patients with genotype 1 chronic hepatitis C. Hepatology Volume 56, Issue 3, pages 850–860, September 2012
11. Shan Liu, Cipriano L, Holodniy M, Owens D.; New Protease Inhibitors for the Treatment of Chronic Hepatitis CA Cost-Effectiveness Analysis. Annals of Internal Medicine. 2012 Feb;156(4):279-290.







